下载高清试卷
【2020-2021学年江苏省苏州市高新区九年级(上)期中化学试卷】-第1页
试卷格式:2020-2021学年江苏省苏州市高新区九年级(上)期中化学试卷.PDF
试卷热词:最新试卷、2020年、江苏试卷、苏州市试卷、化学试卷、九年级上学期试卷、期中试卷、初中试卷
扫码查看解析
试卷题目
1.树立“绿水青山就是金山银山”的理念,建设美丽浙江。下列做法不利于生态修复的是( )
- A. 生活污水﹣集中处理
- B. 农药化肥﹣合理施用
- C. 工业废气﹣净化排放
- D. 废旧电池﹣随手丢弃
2.下列是中国古代四大发明的某一工艺流程或应用,其中属于化学变化的是( )
- A. 火药:烟花燃放
- B. 印刷:活字排版
- C. 造纸:破布捣烂
- D. 司南:航海导向
3.生活中用到的下列物质,属于纯净物的是( )
- A. 温度计中水银
- B. 取暖用的煤炭
- C. 调味用的食醋
- D. 饮料用的果汁
4.生活中常接触到“含氟牙膏”、“富硒茶叶”等用品。这里的氟、硒是指( )
- A. 元素
- B. 原子
- C. 分子
- D. 物质
5.下列人体所缺元素与引起的健康问题,关系错误的是( )
- A. 缺铁会引起贫血症
- B. 缺碘会引起骨质疏松症
- C. 缺钙会引起佝偻病
- D. 缺锌会引起侏儒症
6.下列实验操作中,正确的是( )
- A.
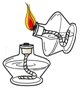 点燃酒精灯
点燃酒精灯 - B.
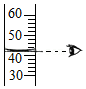 量筒读数
量筒读数 - C.
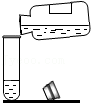 倾倒液体
倾倒液体 - D.
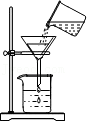 过滤
过滤
7.下列物质由离子构成的是( )
- A. 镁
- B. 氯化钠
- C. 金刚石
- D. 蒸馏水
8.下列物质的性质与用途对应关系错误的是( )
- A. 金刚石硬度大,可制造钻头
- B. 氮气的化学性质不活泼,常用作保护气
- C. 干冰升华吸热,常用于制汽水
- D. 镁燃烧发出耀眼的白光,可作烟花
9.下列物质中氮元素化合价最低的是( )
- A. N2
- B. HNO3
- C. NaNO2
- D. NH4Cl
10.二氧化碳是自然界不可缺少的气体,下列关于二氧化碳的认识不正确的是( )
- A. 二氧化碳和氧气可以通过生态系统实现双循环
- B. CO2能灭火,是因为二氧化碳一般不可燃、不助燃,且密度比空气大
- C. CO2无毒,当空气中的CO2超过正常含量时,不会对人体健康产生影响
- D. 二氧化碳通入紫色石蕊试液变红,是因为二氧化碳能与水反应生成一种酸
11.下列化学符号中数字“2”表示的意义,正确的是( )
- A. 2Au:表示2个金原子
- B. SO2:表示二氧化硫中含有2个氧原子
- C. :表示一个镁离子带2个单位正电荷
+2 Mg - D. S2﹣:表示硫元素的化合价为﹣2价
12.如图所示,甲是溴(Br)的原子结构示意图,乙摘自元素周期表。下列说法正确的是( )
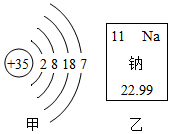

- A. 甲元素属于金属元素
- B. 乙原子的核内中子数为11
- C. 甲原子核外共有5个电子层
- D. 甲、乙两种元素形成化合物的化学式是NaBr
13.下列关于实验现象描述正确的是( )
- A. 在试管中加热铜绿,绿色粉末变黑,试管内壁有水雾
- B. 木炭在氧气中燃烧,发出红光,产生能使澄清石灰水变浑浊的气体
- C. 铁丝在空气中燃烧,火星四射,生成黑色固体
- D. 在空气中灼烧葡萄糖,固体先熔化,后燃烧,留下黑色的炭黑
14.事物的宏观表象是由其微观性质决定的。下列事实及解释中,不正确的是( )
- A. 成熟的菠萝会散发出浓浓的香味,说明分子在不断地运动
- B. 水沸腾时能掀开壶盖,说明分子的大小随温度升高而增大
- C. 50mL水和50mL酒精混合后总体积小于100mL,说明分子间有空隙
- D. 水和过氧化氢的化学性质不同,说明它们的分子结构不同
15.茶叶中含有茶氨酸(C7H14N2O3),它有降低血压、提高记忆力、保护神经细胞等功效。下列说法正确的( )
- A. 茶氨酸由C、H、N、O四种元素组成
- B. 茶氨酸由26个原子构成
- C. 茶氨酸的相对分子质量为174g
- D. 茶氨酸中有一个N2分子
16.下列推理正确的是( )
- A. 分子是构成物质的微粒,所以物质都是由分子构成的
- B. 单质中只含一种元素,所以只含一种元素的纯净物一定是单质
- C. 元素的化学性质与原子核外最外层电子数关系密切,所以核外最外层电子数相同的微粒,对应元素的化学性质一定相同
- D. 同一种元素的微粒具有相同的质子数,所以具有相同的质子数的微粒一定属于同一种元素
17.如图是某密闭容器中物质变化的微观示意图(“●”代表碳原子,“○”代表氧原子),下列有关说法中正确的是( )

①参加反应的分子个数比为1:1
②排列再紧密的分子之间也有空隙
③过程Ⅰ反应类型为化合反应
④过程II发生了物理变化.

①参加反应的分子个数比为1:1
②排列再紧密的分子之间也有空隙
③过程Ⅰ反应类型为化合反应
④过程II发生了物理变化.
- A. ①②
- B. ②③
- C. ①②④
- D. ②③④
18.化学概念间在逻辑上有如图所示的部分关系,下列概念间的关系说法正确的是( )
包含关系: 并列关系:
并列关系: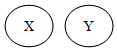 交叉关系:
交叉关系: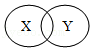
包含关系:
 并列关系:
并列关系: 交叉关系:
交叉关系: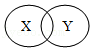
- A. 纯净物与混合物属于包含关系
- B. 单质与化合物属于交叉关系
- C. 化合物与氧化物属于包含关系
- D. 氧化反应与化合反应属于并列关系
19.将一定浓度的稀盐酸、稀硫酸(H2SO4的水溶液)分别加入装有等质量CaCO3粉末的容器中,相同条件下测得两者产生的CO2体积(V)与反应时间(t)的关系如图所示。下列判断错误的是( )
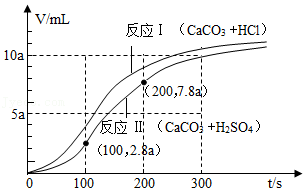

- A. 0~300s内,两个容器内酸的浓度均逐渐减小
- B. 0~100s内,反应Ⅰ、Ⅱ生成CO2的速率均先慢后快
- C. 反应Ⅱ中,0~100s内产生的CO2体积比100~200s内产生的CO2体积少5a mL
- D. 实验室可以用一定浓度的稀硫酸与CaCO3粉末反应制备CO2
20.阅读下面科普短文。
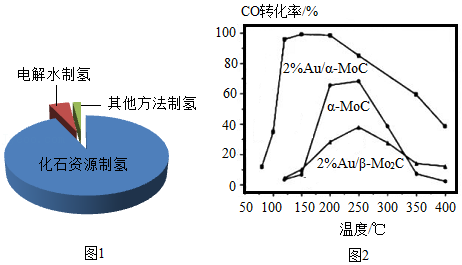
氢能是公认的高热值清洁能源。目前,氢气的来源如图1所示。化石资源制氢最为成熟。水煤气变换反应:CO+H2O
CO2+H2,是化石资源制氢过程中的重要反应之一。北京大学团队研究了在不同温度下,多种催化剂对水煤气变换反应中CO转化率的影响,结果如图2所示。
电解水制氢过程简便,但造价高昂,利用太阳能制氢是未来的发展方向,“人造太阳”的探索也就应运而生。我国的“人造太阳”﹣﹣“东方超环”利用的是核聚变,当氘、氚核聚变温度达到1亿摄氏度、持续时间超过1000秒,就能形成持续反应,为水分解提供能量。2020年4月,“东方超环”实现了1亿摄氏度运行近10秒,取得重大突破。
除了氢气的生产,其运输、储存和利用等仍面临诸多挑战,需要人们不断探索。
依据文章内容回答下列问题。
(1)目前氢气的主要来源是 。
(2)图2中,催化剂为2% Au/a﹣MoC时,CO转化率和温度的关系是 。
(3)根据下表信息可知氘、氚都属于氢元素,理由是 。
(4)
H、
H、
H别表示氢元素的三种原子。可简写成1H、2H、3H。制造燃料电池常用1H,制造氢弹要用2H、3H。2H2与O2反应生成的重水可表示为2H2O。写出3H2在O2中燃烧的符号表达式 。
(5)我国科学家已研制出在新型高效光催化剂作用下,利用太阳能分解水制氢气。水在通过并接触催化剂表面时分解的微观过程如图所示(“〇”表示氢原子,“ ”表示氧原子,“
”表示氧原子,“ ”表示催化剂)。
”表示催化剂)。
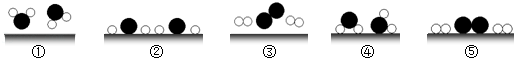
则水分解微观过程的正确顺序是 。
A.④①②③⑤
B.①④②⑤③
C.①④③⑤②
D.③⑤②④①
(6)下列说法正确的是 (填序号)。
A.a﹣MoC可使CO转化率接近100%
B.水电解制氢的不足主要是造价高昂
C.利用太阳能制氢是未来发展方向
D.“东方超环”利用核聚变提供能量

氢能是公认的高热值清洁能源。目前,氢气的来源如图1所示。化石资源制氢最为成熟。水煤气变换反应:CO+H2O
催化剂 |
| 高温 |
电解水制氢过程简便,但造价高昂,利用太阳能制氢是未来的发展方向,“人造太阳”的探索也就应运而生。我国的“人造太阳”﹣﹣“东方超环”利用的是核聚变,当氘、氚核聚变温度达到1亿摄氏度、持续时间超过1000秒,就能形成持续反应,为水分解提供能量。2020年4月,“东方超环”实现了1亿摄氏度运行近10秒,取得重大突破。
除了氢气的生产,其运输、储存和利用等仍面临诸多挑战,需要人们不断探索。
依据文章内容回答下列问题。
(1)目前氢气的主要来源是 。
(2)图2中,催化剂为2% Au/a﹣MoC时,CO转化率和温度的关系是 。
(3)根据下表信息可知氘、氚都属于氢元素,理由是 。
| 原子种类 | 质子数 | 中子数 | 核外电子数 |
| 氘 | 1 | 1 | 1 |
| 氚 | 1 | 2 | 1 |
(4)
| 1 |
| 1 |
| 2 |
| 1 |
| 3 |
| 1 |
(5)我国科学家已研制出在新型高效光催化剂作用下,利用太阳能分解水制氢气。水在通过并接触催化剂表面时分解的微观过程如图所示(“〇”表示氢原子,“
 ”表示氧原子,“
”表示氧原子,“ ”表示催化剂)。
”表示催化剂)。
则水分解微观过程的正确顺序是 。
A.④①②③⑤
B.①④②⑤③
C.①④③⑤②
D.③⑤②④①
(6)下列说法正确的是 (填序号)。
A.a﹣MoC可使CO转化率接近100%
B.水电解制氢的不足主要是造价高昂
C.利用太阳能制氢是未来发展方向
D.“东方超环”利用核聚变提供能量
21.水是生命活动不可缺少的物质。请回答相关的问题。
Ⅰ.探究水的组成实验
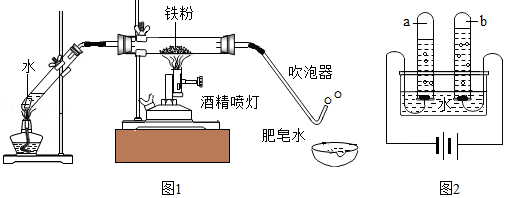
(1)为证明水不是由“水元素”组成的,1785年,拉瓦锡在高温的条件下,用水蒸气与红热的铁反应,将水转化为氢气,同时生成四氧化三铁。模拟实验装置如图1所示。
①该反应的化学符号表达式为 。
②加热铁粉前,应先通入水蒸气一段时间,理由是 。
(2)电解水实验的简易装置如图2所示,b中收集到的气体是 (填化学式);从该实验得到关于水的组成的结论是 ;从能量变化角度看,该过程是将 能转化为化学能。
Ⅱ.水的净化
化学兴趣小组收集了一瓶浑浊的京杭大运河的河水,模拟自来水厂进行水的净化过程。其实验过程如图3所示,请回答以下问题。
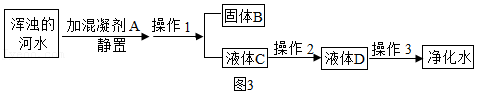
(3)自来水厂常用明矾作絮凝剂,是因为明矾溶于水后生成具有吸附作用的胶状物氢氧化铝,氢氧化铝的化学式为 。
(4)操作2是吸附。主要除去液体C中一些异味和色素,可选用的物质是 。
(5)操作3是消毒杀菌。该过程一般利用液氯汽化后的氯气(双原子分子)与水反应生成盐酸和次氯酸(HClO),该反应的符号表达式是 。
(6)将净化水加热煮沸,发现水壶内有水垢(主要成分为碳酸钙)产生,则加热煮沸除了杀菌消毒之外,还起到的作用是 。欲使净化水转化为纯水,则可采取的方法是 。
Ⅰ.探究水的组成实验

(1)为证明水不是由“水元素”组成的,1785年,拉瓦锡在高温的条件下,用水蒸气与红热的铁反应,将水转化为氢气,同时生成四氧化三铁。模拟实验装置如图1所示。
①该反应的化学符号表达式为 。
②加热铁粉前,应先通入水蒸气一段时间,理由是 。
(2)电解水实验的简易装置如图2所示,b中收集到的气体是 (填化学式);从该实验得到关于水的组成的结论是 ;从能量变化角度看,该过程是将 能转化为化学能。
Ⅱ.水的净化
化学兴趣小组收集了一瓶浑浊的京杭大运河的河水,模拟自来水厂进行水的净化过程。其实验过程如图3所示,请回答以下问题。

(3)自来水厂常用明矾作絮凝剂,是因为明矾溶于水后生成具有吸附作用的胶状物氢氧化铝,氢氧化铝的化学式为 。
(4)操作2是吸附。主要除去液体C中一些异味和色素,可选用的物质是 。
(5)操作3是消毒杀菌。该过程一般利用液氯汽化后的氯气(双原子分子)与水反应生成盐酸和次氯酸(HClO),该反应的符号表达式是 。
(6)将净化水加热煮沸,发现水壶内有水垢(主要成分为碳酸钙)产生,则加热煮沸除了杀菌消毒之外,还起到的作用是 。欲使净化水转化为纯水,则可采取的方法是 。
22.化学小组同学设计了如图所示装置(夹持仪器已略去)做了2个趣味实验。实验时,打开止水夹,C瓶内的水流入D中,使B试管内气压减小,B中长导管口有气泡冒出。
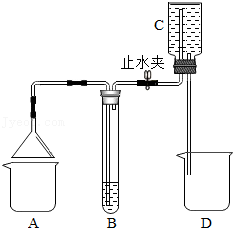
(1)在A处烧杯内放置燃烧的蜡烛,打开止水夹,B中无色溶液变浑浊,B中的试剂是 ,变浑浊的符号表达式为 。
(2)在A处烧杯内放置某无色溶液,打开止水夹。若B中盛有的无色液体变红,则A处烧杯内的液体可能是 ,无色液体B中含有 才会有此现象。

(1)在A处烧杯内放置燃烧的蜡烛,打开止水夹,B中无色溶液变浑浊,B中的试剂是 ,变浑浊的符号表达式为 。
(2)在A处烧杯内放置某无色溶液,打开止水夹。若B中盛有的无色液体变红,则A处烧杯内的液体可能是 ,无色液体B中含有 才会有此现象。
23.如图是实验室常用的实验仪器与装置,根据所学知识回答下列问题:

(1)写出图中对应序号的仪器的名称:① ,② 。
(2)实验室常用高锰酸钾制取氧气。
①高锰酸钾应储存在 (填“广口”或“细口”)试剂瓶中。
②所选用的发生装置是 (填装置序号),该装置还需添加的实验用品为 ,反应的符号表达式为 。
③若用D装置来收集氧气,验证此装置是否集满氧气的方法为 。
(3)“富氧空气”是指氧气含量高于普通空气的气体。在“新冠肺炎”重症患者的治疗上有一个重要环节为“高流氧呼吸”,其本质也和“富氧空气”差不多,化学兴趣小组欲用过氧化氢溶液与二氧化锰混合制取“富氧空气”。
①该反应制取氧气的化学符号表达式 ,该反应的基本反应类型为 反应(填写“化合”或“分解”)。
②如采用装置F,用纯氮气及上述实验制取的氧气,混制一瓶(集气瓶容积为250mL)氧气体积分数为40%的“富氧空气”,气体应从该装置中的管 (选“f”或“g”)通入,先通入氮气排出120mL水,再通入氧气排出 mL水。
(4)通常状况下,氨气是一种无色、有强烈刺激性气味的污染性气体,极易溶解于水形成氨水,相同条件下密度比空气小。实验室可以用氯化铵与熟石灰混合加热制取氨气。请从如图中选出合适的仪器连接成一套制备并收集一瓶氨气的装置。则装置的接口连接顺序是 →h,上述实验中,G装置的作用是 。

(1)写出图中对应序号的仪器的名称:① ,② 。
(2)实验室常用高锰酸钾制取氧气。
①高锰酸钾应储存在 (填“广口”或“细口”)试剂瓶中。
②所选用的发生装置是 (填装置序号),该装置还需添加的实验用品为 ,反应的符号表达式为 。
③若用D装置来收集氧气,验证此装置是否集满氧气的方法为 。
(3)“富氧空气”是指氧气含量高于普通空气的气体。在“新冠肺炎”重症患者的治疗上有一个重要环节为“高流氧呼吸”,其本质也和“富氧空气”差不多,化学兴趣小组欲用过氧化氢溶液与二氧化锰混合制取“富氧空气”。
①该反应制取氧气的化学符号表达式 ,该反应的基本反应类型为 反应(填写“化合”或“分解”)。
②如采用装置F,用纯氮气及上述实验制取的氧气,混制一瓶(集气瓶容积为250mL)氧气体积分数为40%的“富氧空气”,气体应从该装置中的管 (选“f”或“g”)通入,先通入氮气排出120mL水,再通入氧气排出 mL水。
(4)通常状况下,氨气是一种无色、有强烈刺激性气味的污染性气体,极易溶解于水形成氨水,相同条件下密度比空气小。实验室可以用氯化铵与熟石灰混合加热制取氨气。请从如图中选出合适的仪器连接成一套制备并收集一瓶氨气的装置。则装置的接口连接顺序是 →h,上述实验中,G装置的作用是 。
24.某小组在学习“二氧化碳实验室制取的研究”课题时,探究了二氧化碳的收集方法。
【查阅资料】1、通常状况下,1体积水约溶解1体积二氧化碳,所得溶液的pH约为5.6,pH越小,二氧化碳在水中溶解越多。
2、石灰石中的杂质既不和盐酸反应,也不溶于水。
【提出问题】二氧化碳能不能用排水法收集?
【设计实验】
实验一:在通常状况下,测定二氧化碳溶于水所得溶液的pH,判断二氧化碳在水中溶解的体积,如图:

(1)甲装置中反应的化学方程式 。
(2)检查甲装置气密性的方法是 关闭活塞和止水夹K1,打开K2、K3双手握住锥形瓶,观察到 ,说明装置气密性良好。
(3)实验时,需先将甲装置中的空气排尽。其操作是打开止水夹 K1,关闭止水夹 K2,打开活塞,滴加稀盐酸至空气排尽。检验空气排尽的方法是 。
(4)关闭 K1,打开 K2、K3,待丙装置中收集半瓶气体时,关闭K2、K3,充分振荡丙装置,分别测得丙、丁瓶装置中溶液的pH为5.5和6.5.分析可知,溶解的二氧化碳体积丙装置中 (填“大于”或“等于”或“小于”)丁装置中。实验中,乙装置的作用是 。
(5)实验结束后,装置甲反应后溶液中溶质除了氯化钙还有没有其他物质?请设计实验证明你的猜想(写出实验方法、现象和结论)
(6)实验二:用二氧化碳数字传感器测得收集的气体中二氧化碳体积分数。如图是收集的气体中二氧化碳体积分数随时间变化的关系图,从图中能得到哪些信息:
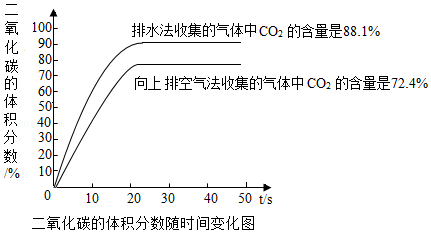
① ,
② 。
(7)【结论反思】由实验一、二分析,改进实验装置,二氧化碳能用排水法收集。能降低二氧化碳在水中溶解性的措施③ ,④
【查阅资料】1、通常状况下,1体积水约溶解1体积二氧化碳,所得溶液的pH约为5.6,pH越小,二氧化碳在水中溶解越多。
2、石灰石中的杂质既不和盐酸反应,也不溶于水。
【提出问题】二氧化碳能不能用排水法收集?
【设计实验】
实验一:在通常状况下,测定二氧化碳溶于水所得溶液的pH,判断二氧化碳在水中溶解的体积,如图:

(1)甲装置中反应的化学方程式 。
(2)检查甲装置气密性的方法是 关闭活塞和止水夹K1,打开K2、K3双手握住锥形瓶,观察到 ,说明装置气密性良好。
(3)实验时,需先将甲装置中的空气排尽。其操作是打开止水夹 K1,关闭止水夹 K2,打开活塞,滴加稀盐酸至空气排尽。检验空气排尽的方法是 。
(4)关闭 K1,打开 K2、K3,待丙装置中收集半瓶气体时,关闭K2、K3,充分振荡丙装置,分别测得丙、丁瓶装置中溶液的pH为5.5和6.5.分析可知,溶解的二氧化碳体积丙装置中 (填“大于”或“等于”或“小于”)丁装置中。实验中,乙装置的作用是 。
(5)实验结束后,装置甲反应后溶液中溶质除了氯化钙还有没有其他物质?请设计实验证明你的猜想(写出实验方法、现象和结论)
(6)实验二:用二氧化碳数字传感器测得收集的气体中二氧化碳体积分数。如图是收集的气体中二氧化碳体积分数随时间变化的关系图,从图中能得到哪些信息:

① ,
② 。
(7)【结论反思】由实验一、二分析,改进实验装置,二氧化碳能用排水法收集。能降低二氧化碳在水中溶解性的措施③ ,④
25.84消毒液是一种无色或者淡黄色具有刺激性气味的含氯消毒剂,有效成分为次氯酸钠(NaClO)。广泛用于医院、宾馆、旅游、家庭等的卫生消毒。某化学兴趣小组对该消毒液进行了如下系列探究。
【查阅资料】
84消毒液不稳定,其杀菌作用主要依靠有效氯,有效氯越高杀菌效果越好。
探究一:84消毒液中有效氯含量的稳定性。
0.5%的84消毒液在不同温度、不同存放时间下的有效氯含量:
(1)【解释与结论】
综合分析探究一中数据,在其他条件不变时,0.5%的84消毒液有效氯存留率受温度和时间的影响,其影响的变化趋势是 ,因此保存84消毒液应注意的问题是 。
探究二:84消毒液、H2O2溶液都是常用消毒剂,兴趣小组对两种消毒剂进行了如下探究活动。
(2)【实验1】取少量84消毒液于试管中,滴加H2O2溶液,发现有大量气泡产生;然后 , (分别填写实验操作和现象),证明产生的气体是氧气。
【提出问题】在上述反应中,NaClO的作用是什么?
(3)【作出猜想】猜想一:作反应物,NaClO与H2O2溶液发生化学反应;
猜想二:作 ,具有类似分解H2O2溶液制氧气时MnO2的作用。
【实验2】
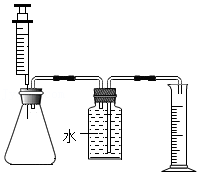
①按如图所示组装实验装置,并检查装置气密性。

②向锥形瓶中加入30mL 84消毒液,注射器中吸入25mL H2O2溶液。
③将注射器中的H2O2溶液平均分5次推入锥形瓶中:每次推入H2O2溶液,待不再产生气泡后,记录收集气体的总体积(忽略其他因素对测量结果造成的影响)见下表。
(4)分析表中数据得出“猜想一正确”,其依据是 。
(5)表中的数据x= 。
(6)【分析讨论】NaClO与H2O2溶液反应除生成氧气外,还生成氯化钠和水,该反应的符号表达式为 。
(7)【拓展反思】生活中常用消毒剂除84消毒液、H2O2溶液外,还有75%酒精等。在使用各种消毒剂时,要考虑它们的性质。切记:科学使用,注意安全!生活中下列使用消毒剂的做法正确的是 。
A.不同的消毒剂都可随意混合使用
B.使用84消毒液的温度越高效果越好
C.使用75%酒精消毒应远离明火,防止火灾
D.H2O2溶液、75%酒精等消毒剂均应密封保存

【查阅资料】
84消毒液不稳定,其杀菌作用主要依靠有效氯,有效氯越高杀菌效果越好。
探究一:84消毒液中有效氯含量的稳定性。
0.5%的84消毒液在不同温度、不同存放时间下的有效氯含量:
| 存放时间 (小时) | 不同温度下,有效氯存留率 | |||
| 60℃ | 70℃ | 80℃ | 90℃ | |
| 0(对照) | 100% | 100% | 100% | 100% |
| 3.0 | …… | …… | 94.66% | 88.05% |
| 6.0 | …… | 96.66% | 89.67% | 74.69% |
| 12.0 | …… | 93.32% | 82.62% | …… |
| 20.0 | 94.75% | …… | …… | …… |
| 20.0 | 92.99% | …… | …… | …… |
(1)【解释与结论】
综合分析探究一中数据,在其他条件不变时,0.5%的84消毒液有效氯存留率受温度和时间的影响,其影响的变化趋势是 ,因此保存84消毒液应注意的问题是 。
探究二:84消毒液、H2O2溶液都是常用消毒剂,兴趣小组对两种消毒剂进行了如下探究活动。
(2)【实验1】取少量84消毒液于试管中,滴加H2O2溶液,发现有大量气泡产生;然后 , (分别填写实验操作和现象),证明产生的气体是氧气。
【提出问题】在上述反应中,NaClO的作用是什么?
(3)【作出猜想】猜想一:作反应物,NaClO与H2O2溶液发生化学反应;
猜想二:作 ,具有类似分解H2O2溶液制氧气时MnO2的作用。
【实验2】
①按如图所示组装实验装置,并检查装置气密性。

②向锥形瓶中加入30mL 84消毒液,注射器中吸入25mL H2O2溶液。
③将注射器中的H2O2溶液平均分5次推入锥形瓶中:每次推入H2O2溶液,待不再产生气泡后,记录收集气体的总体积(忽略其他因素对测量结果造成的影响)见下表。
| 第1次 | 第2次 | 第3次 | 第4次 | 第5次 | |
| 收集气体的总体积/mL | 140 | 280 | 365 | x | 365 |
(4)分析表中数据得出“猜想一正确”,其依据是 。
(5)表中的数据x= 。
(6)【分析讨论】NaClO与H2O2溶液反应除生成氧气外,还生成氯化钠和水,该反应的符号表达式为 。
(7)【拓展反思】生活中常用消毒剂除84消毒液、H2O2溶液外,还有75%酒精等。在使用各种消毒剂时,要考虑它们的性质。切记:科学使用,注意安全!生活中下列使用消毒剂的做法正确的是 。
A.不同的消毒剂都可随意混合使用
B.使用84消毒液的温度越高效果越好
C.使用75%酒精消毒应远离明火,防止火灾
D.H2O2溶液、75%酒精等消毒剂均应密封保存
26.某学习小组对人体呼出气体的成分进行探究
【知识回顾】
(1)供给生物呼吸是氧气的一个重要用途,吸入的空气中氧气的体积分数约为 。
(2)红磷在空气中燃烧的符号表达式为 。
【粗略测量】
(3)检查装置气密性。在医用输液袋中装入VmL呼出气体。如图一所示,集气瓶中装入VmL足量NaOH溶液以充分吸收CO2,带孔燃烧匙内装入足量红磷(通常条件下,红磷与NaOH溶液不反应)。连接成如图二所示装置,则方框内最合适的装置是 (在图一中选择)。
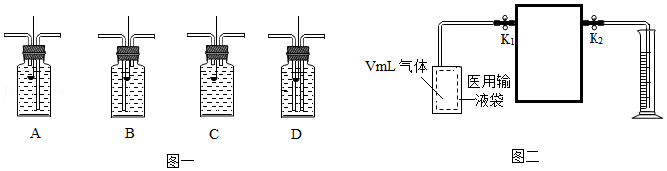
打开弹簧夹K1、K2,缓慢将袋中的气体全部排出。读出量筒中液体体积为V1mL。
(4)关闭弹簧夹K1、K2,用激光笔照射红磷,红磷剧烈燃烧。待装置和气体 ,打开K2,读出量筒中液体体积为V2mL。
(5)数据分析:人体呼出气体中,氧气的体积分数可表示为 ×100%;若数据
×100%满足 的条件,则理论上可证明呼吸作用产生了CO2
【精密测定】
如图三所示,把O2、CO2、湿度(测水蒸气)传感器探头放入有少量空气的保鲜袋中,打开仪器开始采集数据,然后向袋内呼出气体。采集的数据食品如图四所示,纵坐标均为某气体体积分数(%),横坐标均为时间(S)。据图回答:
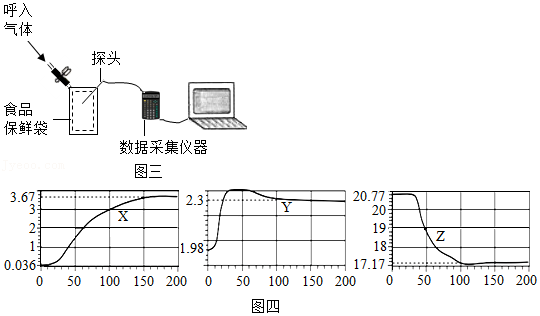
(6)表示O2体积分数变化的曲线是 (选填“X”、“Y”、“Z”)。
(7)实验中,200s时没有采集数据的其余气体的总体积分数为 。
(8)Y曲线60s之后逐渐下降,可推测保鲜袋中可能出现的现象是 。
【反思拓展】
(9)小组同学曾认为空气成分中“其它气体和杂质”主要包括水蒸气等,由实验可判断该认识是错误的,理由是 。
(10)为了能保持载人飞行的飞船座舱内空气成分的稳定,科学家设想的方案是:不断把座舱内空气通过盛有过氧化钠的容器,并把处理后的气体重新充入座舱。其中过氧化钠的作用是 。
【知识回顾】
(1)供给生物呼吸是氧气的一个重要用途,吸入的空气中氧气的体积分数约为 。
(2)红磷在空气中燃烧的符号表达式为 。
【粗略测量】
(3)检查装置气密性。在医用输液袋中装入VmL呼出气体。如图一所示,集气瓶中装入VmL足量NaOH溶液以充分吸收CO2,带孔燃烧匙内装入足量红磷(通常条件下,红磷与NaOH溶液不反应)。连接成如图二所示装置,则方框内最合适的装置是 (在图一中选择)。

打开弹簧夹K1、K2,缓慢将袋中的气体全部排出。读出量筒中液体体积为V1mL。
(4)关闭弹簧夹K1、K2,用激光笔照射红磷,红磷剧烈燃烧。待装置和气体 ,打开K2,读出量筒中液体体积为V2mL。
(5)数据分析:人体呼出气体中,氧气的体积分数可表示为 ×100%;若数据
| V-V1 |
| V |
【精密测定】
如图三所示,把O2、CO2、湿度(测水蒸气)传感器探头放入有少量空气的保鲜袋中,打开仪器开始采集数据,然后向袋内呼出气体。采集的数据食品如图四所示,纵坐标均为某气体体积分数(%),横坐标均为时间(S)。据图回答:

(6)表示O2体积分数变化的曲线是 (选填“X”、“Y”、“Z”)。
(7)实验中,200s时没有采集数据的其余气体的总体积分数为 。
(8)Y曲线60s之后逐渐下降,可推测保鲜袋中可能出现的现象是 。
【反思拓展】
(9)小组同学曾认为空气成分中“其它气体和杂质”主要包括水蒸气等,由实验可判断该认识是错误的,理由是 。
(10)为了能保持载人飞行的飞船座舱内空气成分的稳定,科学家设想的方案是:不断把座舱内空气通过盛有过氧化钠的容器,并把处理后的气体重新充入座舱。其中过氧化钠的作用是 。
查看全部题目
相关试卷推荐
更多热门试卷
如何查看答案以及解析
扫描右侧二维码查看试卷答案解析以及视频讲解