下载高清试卷
【2018年湖南省株洲市中考化学试卷】-第1页
试卷格式:2018年湖南省株洲市中考化学试卷.PDF
试卷热词:最新试卷、2018年、湖南试卷、株洲市试卷、化学试卷、九年级试卷、中考试卷、初中试卷
扫码查看解析
试卷题目
1.下列过程中一定发生了化学变化的是( )
- A. 碘升华
- B. 铜生锈
- C. 研磨固体
- D. 海水晒盐
2.下列物质中属于碱的是( )
- A. 食用碱
- B. 烧碱
- C. 纯碱
- D. 生石灰
3.下列有关化学实验操作的图示中正确的是( )
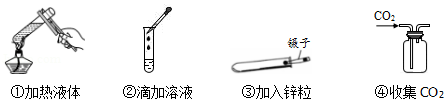

- A. ①②
- B. ②④
- C. ③④
- D. ③
4.某小孩经常贫血,该小孩可能缺少的元素是( )
- A. Fe
- B. Ca
- C. Zn
- D. F
5.下列加点元素的化合价为+5价的是( )
- A. H N O2
- B. Na C lO3
- C. K M nO4
- D. F eCl3
6.已知在相同的温度和压强下,气体的扩散速率与其相对分子质量的平方根成反比。下列气体中扩散速率最小的是( )
- A. 氢气
- B. 氮气
- C. 氯气
- D. 二氧化硫
7.2018年6月14日俄罗斯世界足球赛拉开序幕,32支足坛劲旅争夺“大力神杯”。“大力神杯”由18K黄金打造,重达6kg。金的元素符号为( )
- A. Ac
- B. Au
- C. As
- D. At
8.2018年5月18~19日全国生态环境保护大会在北京举行。习近平主席在会上强调:坚决打好污染防治攻坚战,推动我国生态文明建设迈上新台阶。下列措施会引起环境污染的是( )
- A. 大量直接焚烧生活垃圾
- B. 用人畜粪便等废弃物制得甲烷作燃料
- C. 将煤脱硫后再综合利用
- D. 大力推广使用太阳能、风能等绿色能源
9.下列反应中属于复分解反应的是( )
- A. BaCl2+2AgNO3═Ba(NO3)2+2AgCl↓
- B. 2NaCl+2H2O2NaOH+H2↑+Cl2↑
通电 - C. Fe2O3+3CO2Fe+3CO2
高温 - D. 2Mg+CO22MgO+C
点燃
10.常温下,一些饮料或食物的近似pH如下:
下列说法中不正确的是( )
| 食品 | 苹果汁 | 苏打水 | 牛奶 | 鸡蛋清 |
| pH | 2.9~3.3 | 8.1~8.4 | 6.3~6.6 | 7.6~8.0 |
下列说法中不正确的是( )
- A. 牛奶和苹果汁都显酸性
- B. 牛奶比苹果汁的酸性强
- C. 苏打水和鸡蛋清都显碱性
- D. 苏打水比鸡蛋清的碱性强
11.下列说法中正确的是( )
- A. 含碳的化合物都是有机化合物
- B. 塑料、纤维、橡胶全都是合成有机高分子化合物
- C. 使用一些新型的、可降解的塑料能缓解“白色污染”问题
- D. 人们在日常生活中可通过加肥皂水的方法来降低水的硬度
12.碘元素在元素周期表中的信息如图。下列说法正确的是( )
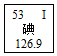

- A. 1个碘原子中含有53个中子
- B. 碘元素属于金属元素
- C. 1个I2分子中含有53个电子
- D. 碘的相对原子质量为126.9
13.下列有关“燃烧和灭火”的说法中不正确的是( )
- A. 用水灭火是降低了物质的着火点
- B. 加油站、油库必须严禁烟火
- C. 点燃可燃性气体前一定要验纯
- D. 灭火的原理之一是隔绝空气
14.如图表示两种气体发生化学反应,其中相同的球代表同种原子。下列说法中正确的是( )


- A. 该示意图中有四种分子
- B. 该反应表示H2与O2化合生成水
- C. 化学反应前后分子的种类不变
- D. 原子在化学反应中不可再分
15.化学与生产、生活息息相关,下列说法中不正确的是( )
- A. 为了减少污染,应根据作物、虫害和农药的特点按规定合理施用农药
- B. 服用含氢氧化铝[Al(OH)3]的药物可以治疗胃酸过多症
- C. 农业上铵态氮肥不宜与熟石灰混合使用
- D. 日常生活中用含碳酸钠的发酵粉来焙制糕点
16.下列说法正确的是( )
- A. 用甲醛水溶液浸泡过的海鲜可以长时间保存而不变质,人们可以放心食用
- B. 糖类、蛋白质、油脂都是只由C、H、O三种元素组成的有机高分子化合物
- C. 食物中的淀粉在人体内经酶的催化作用,与水发生一系列反应,最终变成葡萄糖
- D. 维生素可以起到维持身体健康的重要作用,缺乏维生素C会引起夜盲症
17.下列物质中,不能使氧化铜还原成铜单质的是( )
- A. 一氧化碳
- B. 木炭
- C. 氢气
- D. 氧气
18.与化学相关的知识常见于中国传统文化典籍之中。下列有关说法不正确的是( )
- A. “熬胆矾铁釜,久之亦化为铜”,该过程发生了置换反应
- B. 某古剑“以剂钢为刃,铁为茎干……”,“剂钢”指的是铁的合金
- C. 《梦溪笔谈》载:“高奴县出脂水,燃之如麻,但烟甚浓。”所述“脂水”属于石油
- D. 《肘后备急方》载:“青蒿一握,以水二升渍,绞取汁”。此提取青蒿素的方法属蒸馏
19.下列实验操作和目的都正确的是( )
| 选项 | 操作 | 目的 |
| A | 将一小片pH试纸润湿后放在玻璃片上,用玻璃棒蘸取溶液滴到pH试纸上 | 测定某溶液的pH |
| B | 制取蒸馏水时,应加入几粒沸石(或碎瓷片) | 防止加热时出现暴沸 |
| C | 先将胶头滴管挤压,再伸入试剂中吸取液体 | 保证滴管的胶头部分也充满液体 |
| D | 将水沿烧杯壁缓慢地注入盛有浓硫酸的烧杯里,并用玻璃棒不断搅拌 | 稀释浓硫酸 |
- A. A
- B. B
- C. C
- D. D
20.已知硫酸钠(Na2SO4)与硫酸钾(K2SO4)的固体混合物中,钠元素的质量分数为a%,钾元素的质量分数为b%,则混合物中氧元素的质量分数为
( )
( )
- A.
2(1-a%-b%) 3 - B.
1-a%-b% 3 - C.
1-a%-b% 6 - D. 无法计算
21.请用化学符号填空:
(1)铝离子 ;(2)小苏打 ;(3)三氧化硫 。
(1)铝离子 ;(2)小苏打 ;(3)三氧化硫 。
22.图中A、B、C、D为四种元素原子的结构示意图。请回答下列问题:

(1)B、D两种原子相互结合形成的化合物的化学式为 (填元素符号表示的化学式)。
(2)以上结构示意图中, (填字母代号)表示的是金属元素的原子。
(3)D中x= 。

(1)B、D两种原子相互结合形成的化合物的化学式为 (填元素符号表示的化学式)。
(2)以上结构示意图中, (填字母代号)表示的是金属元素的原子。
(3)D中x= 。
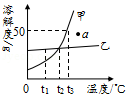
23.如图为甲和乙两种固体物质的溶解度曲线。回答下列问题:
(1)当温度为 时,甲、乙两种物质的饱和溶液中溶质的质量分数相等。
(2)图中a点对应的甲溶液是 (填“饱和”或“不饱和”)溶液。
(3)当温度为t3℃时,要将质量分数为20%的甲溶液100g变成饱和溶液,需要加入 g甲固体(不含结晶水)。
(1)当温度为 时,甲、乙两种物质的饱和溶液中溶质的质量分数相等。
(2)图中a点对应的甲溶液是 (填“饱和”或“不饱和”)溶液。
(3)当温度为t3℃时,要将质量分数为20%的甲溶液100g变成饱和溶液,需要加入 g甲固体(不含结晶水)。

24.“宏观辨识与微观探析”是中学化学学科核心素养之一。现向一支盛有少量的硫酸铜溶液的试管中滴加足量的氢氧化钠溶液。
(1)可观察到的宏观现象是:有 色沉淀生成;溶液由蓝色逐渐变为无色。
(2)从微观层面分析,沉淀是Cu2+与OH﹣相互结合生成了不溶于水的物质;溶液颜色的变化是因为 。
(3)上述反应可以用化学方程式表示为: 。
(1)可观察到的宏观现象是:有 色沉淀生成;溶液由蓝色逐渐变为无色。
(2)从微观层面分析,沉淀是Cu2+与OH﹣相互结合生成了不溶于水的物质;溶液颜色的变化是因为 。
(3)上述反应可以用化学方程式表示为: 。
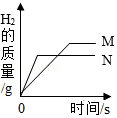
25.现有相同质量且相同形状的锌和铁两种金属,分别加入足量的溶质质量分数相同的稀硫酸中,产生氢气的质量与反应时间的关系如图所示。
(1)图中M代表 (填“铁”或“锌”)。
(2)请写出锌和铁两种金属中与稀硫酸反应速率较快的化学方程式: 。
(1)图中M代表 (填“铁”或“锌”)。
(2)请写出锌和铁两种金属中与稀硫酸反应速率较快的化学方程式: 。

26.某化学活动小组在实验室以MnO2固体为原料制取少量MnCO3,基本流程如下:

已知:MnSO4与MnCl2都可溶于水;MnCO3难溶于水且在100℃时开始分解。
(1)反应①为化合反应,产物为MnSO4。该反应的化学方程式为 ,下列物质中不能与MnSO4反应的有 。
A、稀硫酸 B、BaCl2 C、盐酸 D、Na2CO3
(2)操作a要用到的实验用品中,除玻璃仪器外,还有 (填具体的实验用品)。
(3)产品MnCO3(Ⅱ) 比MnCO3(Ⅰ) 更纯净,原因是产品MnCO3(Ⅰ) 经过洗涤、烘干以后,表面附着的H2O及 (填化学式)等杂质已被除去。
(4)为获得纯净MnCO3,烘干时需要控制的条件是 。

已知:MnSO4与MnCl2都可溶于水;MnCO3难溶于水且在100℃时开始分解。
(1)反应①为化合反应,产物为MnSO4。该反应的化学方程式为 ,下列物质中不能与MnSO4反应的有 。
A、稀硫酸 B、BaCl2 C、盐酸 D、Na2CO3
(2)操作a要用到的实验用品中,除玻璃仪器外,还有 (填具体的实验用品)。
(3)产品MnCO3(Ⅱ) 比MnCO3(Ⅰ) 更纯净,原因是产品MnCO3(Ⅰ) 经过洗涤、烘干以后,表面附着的H2O及 (填化学式)等杂质已被除去。
(4)为获得纯净MnCO3,烘干时需要控制的条件是 。
27.请用所学的知识回答下列问题:
(1)能产生温室效应的气体中,除二氧化碳以外,还有什么气体?
(2)人类为什么要生产营养强化食品?
(1)能产生温室效应的气体中,除二氧化碳以外,还有什么气体?
(2)人类为什么要生产营养强化食品?
28.我国古代曾用“地糠法”制取Cl2,两用Cl2与石灰乳反应生产漂白粉,流程如下:

已知:漂白粉的有效成分是Ca(ClO)2,Ca(ClO)2的化学名称叫做次氯酸钙。Ca(ClO)2中,氯元素的化合价为+1价。请回答下列问题:
(1)HCl与O2反应的化学方程式为 ,该反应所属的基本反应类型为 。
(2)Ca(ClO)2在物质的分类上属于 。
A、氧化物 B、酸 C、碱 D、盐
(3)“84消毒液”(主要成分为次氯酸钠)与“洁厕灵”(主要成分为盐酸) 不能混合使用,否则会产生氯气使人中毒。请写出次氯酸钠的化学式 。
(4)石灰乳 (填“属于”或“不属于”)溶液。

已知:漂白粉的有效成分是Ca(ClO)2,Ca(ClO)2的化学名称叫做次氯酸钙。Ca(ClO)2中,氯元素的化合价为+1价。请回答下列问题:
(1)HCl与O2反应的化学方程式为 ,该反应所属的基本反应类型为 。
(2)Ca(ClO)2在物质的分类上属于 。
A、氧化物 B、酸 C、碱 D、盐
(3)“84消毒液”(主要成分为次氯酸钠)与“洁厕灵”(主要成分为盐酸) 不能混合使用,否则会产生氯气使人中毒。请写出次氯酸钠的化学式 。
(4)石灰乳 (填“属于”或“不属于”)溶液。
29.在实验室中,我们常用如图所示装置制取和收集某些气体。

(1)写出a、b两种仪器的名称:a为 ,b为 。
(2)实验室用加热高锰酸钾的方法制取氧气时,有两种不同的操作:①先装入药品,后检查装置的气密性;②先检查装置的气密性,后装入药品。你觉得更合理的操作是 (填“①”或“②”)。
(3)氨气(NH3)极易溶于水,在实验室可用氯化铵固体与消石灰粉末混合加热来制取氨气,若要制取并收集一瓶氨气,应选择的装置是 (填图中装置对应的字母)。
(4)在实验室,通常用块状大理石与稀盐酸反应来制取二氧化碳气体,其中稀盐酸不宜用稀硫酸代替的原因 (填“是”或“不是”)因为碳酸钙与稀硫酸不反应。
(5)图示装置B (填“能”或“不能”)用来制取氢气。

(1)写出a、b两种仪器的名称:a为 ,b为 。
(2)实验室用加热高锰酸钾的方法制取氧气时,有两种不同的操作:①先装入药品,后检查装置的气密性;②先检查装置的气密性,后装入药品。你觉得更合理的操作是 (填“①”或“②”)。
(3)氨气(NH3)极易溶于水,在实验室可用氯化铵固体与消石灰粉末混合加热来制取氨气,若要制取并收集一瓶氨气,应选择的装置是 (填图中装置对应的字母)。
(4)在实验室,通常用块状大理石与稀盐酸反应来制取二氧化碳气体,其中稀盐酸不宜用稀硫酸代替的原因 (填“是”或“不是”)因为碳酸钙与稀硫酸不反应。
(5)图示装置B (填“能”或“不能”)用来制取氢气。
30.某校九年级“我们爱化学”活动小组的同学,在探究碱的化学性质时,完成了如图所示的A、B两个实验。请你回答下列问题:

(1)A实验中酚酞的作用是 ,所发生的化学反应方程式为 。
(2)B实验中可观察到的现象是 。
(3)实验后,将两支试管中的废液都倒入废液杯C中,发现混合废液浑浊并显红色。
【分析思考】同学们经过思考一致认为,混合废液显红色是B实验后试管中的溶质与A实验后试管中的酚酞反应的结果。
【提出问题】B实验后试管中的溶质是什么?
【作出猜想】猜想一:试管中的溶质是NaOH;猜想二:试管中的溶质是 ;
猜想三:试管中的溶质是Ca(OH)2和NaOH。
【实验验证】华雪同学利用废液杯C中的混合废液来确定B实验后试管中的溶质:将一定质量的废液过滤,取10g滤液并向其中逐滴加入质量分数为7.3% 的稀盐酸,当加入稀盐酸的质量为20g时反应完全,继续加入稀盐酸,气体的质量不再增加,根据反应现象得到如图所示的图象。
【查阅资料】碳酸钠溶液与稀盐酸的反应是分步进行的。首先是碳酸钠与稀盐酸反应生成碳酸氢钠和氯化钠:Na2CO3+HCl═NaHCO3+NaCl;然后是生成的碳酸氢钠与稀盐酸反应生成氯化钠、二氧化碳气体和水:NaHCO3+HCl═NaCl+CO2↑+H2O。
【实验结论】定性结论:分析图象得出:猜想二是正确的,产生的气体是 (填化学式);猜想一和猜想三是错误的,原因是 。
定量结论:10g废液中含有 g NaOH, g Na2CO3。
【拓展提升】请另外设计一个实验,定性证明上述猜想二是正确的: 。

(1)A实验中酚酞的作用是 ,所发生的化学反应方程式为 。
(2)B实验中可观察到的现象是 。
(3)实验后,将两支试管中的废液都倒入废液杯C中,发现混合废液浑浊并显红色。
【分析思考】同学们经过思考一致认为,混合废液显红色是B实验后试管中的溶质与A实验后试管中的酚酞反应的结果。
【提出问题】B实验后试管中的溶质是什么?
【作出猜想】猜想一:试管中的溶质是NaOH;猜想二:试管中的溶质是 ;
猜想三:试管中的溶质是Ca(OH)2和NaOH。
【实验验证】华雪同学利用废液杯C中的混合废液来确定B实验后试管中的溶质:将一定质量的废液过滤,取10g滤液并向其中逐滴加入质量分数为7.3% 的稀盐酸,当加入稀盐酸的质量为20g时反应完全,继续加入稀盐酸,气体的质量不再增加,根据反应现象得到如图所示的图象。
【查阅资料】碳酸钠溶液与稀盐酸的反应是分步进行的。首先是碳酸钠与稀盐酸反应生成碳酸氢钠和氯化钠:Na2CO3+HCl═NaHCO3+NaCl;然后是生成的碳酸氢钠与稀盐酸反应生成氯化钠、二氧化碳气体和水:NaHCO3+HCl═NaCl+CO2↑+H2O。
【实验结论】定性结论:分析图象得出:猜想二是正确的,产生的气体是 (填化学式);猜想一和猜想三是错误的,原因是 。
定量结论:10g废液中含有 g NaOH, g Na2CO3。
【拓展提升】请另外设计一个实验,定性证明上述猜想二是正确的: 。
31.别嘌醇片(C5H4N4O)可用于治疗因尿酸生成过多而引起的高尿酸血症;非布司他片(C16H16N2O3S)是目前治疗痛风高尿酸血症比较好的一种药物,在临床上非布司他片适用于痛风患者高尿酸血症的长期治疗。
(1)C5H4N4O的相对分子质量为 。
(2)C5H4N4O和C16H16N2O3S中,氮元素的质量分数较大的是 。
(1)C5H4N4O的相对分子质量为 。
(2)C5H4N4O和C16H16N2O3S中,氮元素的质量分数较大的是 。
32.某化学课外活动小组的同学为了测定某氮化镁样品中Mg3N2的质量分数,他们取氮化镁样品5.0g于烧杯中,加入100g某浓度的盐酸(足量),充分反应后(杂质不溶于水也不与盐酸反应),测得剩余固体的质量为1.0g。请计算:
(1)已知:Mg3N2与盐酸反应的生成物只有氯化镁和氯化铵,则在配平的该化学反应方程式中,HCl前面的化学计量数为 。
(2)氮化镁样品中Mg3N2的质量分数。(写出计算过程)
(3)此时所得溶液中氯化镁的质量分数。(写出计算过程)
(1)已知:Mg3N2与盐酸反应的生成物只有氯化镁和氯化铵,则在配平的该化学反应方程式中,HCl前面的化学计量数为 。
(2)氮化镁样品中Mg3N2的质量分数。(写出计算过程)
(3)此时所得溶液中氯化镁的质量分数。(写出计算过程)
查看全部题目