下载高清试卷
【2019年四川省宜宾市中考化学试卷】-第1页
试卷格式:2019年四川省宜宾市中考化学试卷.PDF
试卷热词:最新试卷、2019年、四川试卷、宜宾市试卷、化学试卷、九年级试卷、中考试卷、初中试卷
扫码查看解析
试卷题目
1.“燃面”是宜宾人喜爱的食物,下列有关食材的主要成分为糖类的是( )
- A. 面粉
- B. 花生仁
- C. 食盐
- D. 植物油
2.下列有关物质在其应用中发生了化学变化的是( )
- A. 用铁水铸成锅
- B. 用小苏打治疗胃酸过多症
- C. 用稀有气体制造霓虹灯
- D. 用活性炭除去冰箱中的异味
3.下列有关原子、分子和离子的表述错误的是( )
- A. 湿衣服晾干是分子运动的结果
- B. 氢原子核内只含有质子,无中子
- C. 钠离子中:质子数=核外电子数
- D. 铝原子的结构示意图:
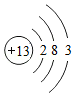
4.对下列各组物质的判断错误的是( )
- A. SO2与SO3﹣﹣组成元素相同
- B. CO与N2﹣﹣相对分子质量相同
- C. C2H4与C3H6﹣﹣碳元素质量分数相等
- D. NaNO3与KMnO4﹣﹣氮元素与锰元素的化合价相同
5.各图中表示氧化物的是( )
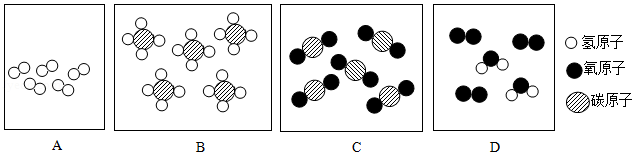

- A. A
- B. B
- C. C
- D. D
6.倡导绿色化学理念,保护环境,人人有责。下列做法错误的是( )
- A. 回收利用废旧金属、废弃塑料
- B. 研制并推广使用可降解塑料制品
- C. 提高化工生产中原料的利用率,减少有害物质排放
- D. 露天焚烧植物秸秆,将得到的草木灰用作肥料
7.下列说法正确的是( )
- A. 生石灰与水反应时吸收热量
- B. 点燃氢气前必须检验其纯度
- C. 硫在氧气中燃烧火焰呈淡蓝色
- D. 用Zn粉与MgSO4溶液反应制取Mg
8.下列反应属于置换反应的是( )
- A. 2H2+O22H2O
点燃 - B. 2Mg+CO22MgO+C
点燃 - C. 3CO+Fe2O32Fe+3CO2
高温 - D. CaCO3+2HCl═CaCl2+CO2↑+H2O
9.下列说法正确的是( )

- A. 水灭火的主要原理是水吸热降低了可燃物的着火点
- B. 用蒸馏的操作净化水不能降低水的硬度
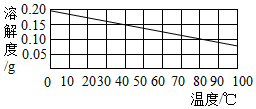
- C. 根据如图可知,降温可使氢氧化钙饱和溶液变为不饱和溶液
- D. 20℃时,KCl的溶解度为34g,该温度下,100g KCl饱和溶液中溶质KCl的质量为34g
10.酸与碱作用生成盐和水的反应叫做中和反应。如图是室温下稀硫酸与氢氧化钠溶液反应过程中的pH变化曲线。下列有关说法正确的是( )
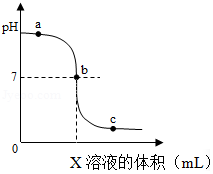

- A. 图中X是氢氧化钠
- B. 向图中a点所示溶液中加入几滴紫色石蕊溶液后,溶液变红
- C. 向图中c点所示溶液中加入铁粉后,溶液中有气泡产生
- D. 稀硫酸与氢氧化钠溶液反应的化学方程式为:H2SO4+2NaOH═Na2SO4+H2O
11.用化学用语填空:
(1)2个磷原子: ;
(2)氯化氢分子: ;
(3)5个铵根离子: ;
(4)硫酸铝: ;
(5)磁铁矿的主要成分: 。
(1)2个磷原子: ;
(2)氯化氢分子: ;
(3)5个铵根离子: ;
(4)硫酸铝: ;
(5)磁铁矿的主要成分: 。
12.X、Y、Z、W、Q、R为初中化学中的常见物质,分别由H、C、O和Cu四种元素中的一种或两种组成。X能与Y在加热条件下发生反应生成W和Q.X是一种黑色固体,溶于硫酸后所得溶液呈蓝色。Q是一种最常用的溶剂。Y、R均是还原性的非金属单质。Z极易与血液中的血红蛋白结合,使人体中毒。回答下列问题:
(1)X的化学式为 。
(2)W的用途: (填一种)。
(3)上述六种物质中可用作燃料的是 (填化学式),其中 的燃烧产物无污染,被认为是理想的清洁、高能燃料。
(4)Q与R在高温下反应生成上述物质中的 (填化学式)和Y。
(1)X的化学式为 。
(2)W的用途: (填一种)。
(3)上述六种物质中可用作燃料的是 (填化学式),其中 的燃烧产物无污染,被认为是理想的清洁、高能燃料。
(4)Q与R在高温下反应生成上述物质中的 (填化学式)和Y。
13.酸雨有很大的危害,能直接破坏农作物、森林,使土壤、湖泊酸化,还能加速建筑物、桥梁、电缆等的腐蚀。回答下列问题:
(1)形成酸雨的主要物质是 ;酸雨的pH (填“大于”、“小于”或“等于”)5.6。
(2)某学校课外活动小组的同学取刚降到地面的雨水水样,每隔几分钟测一次pH,得到数据如表所示:
已知:SO2能与水反应生成H2SO3,H2SO3不稳定,在空气中可被O2氧化成H2SO4.此外,在空气中,粉尘作催化剂,SO2还能被O2氧化成SO3,SO3也可与水反应生成H2SO4,H2SO4的酸性比H2SO3强。
①写出H2SO3与O2反应的化学方程式: 。
②在测定期间雨水的酸性 (填“增强”或“减弱”),其主要原因是 。
(1)形成酸雨的主要物质是 ;酸雨的pH (填“大于”、“小于”或“等于”)5.6。
(2)某学校课外活动小组的同学取刚降到地面的雨水水样,每隔几分钟测一次pH,得到数据如表所示:
| 测定时刻 | 5:05 | 5:10 | 5:15 | 5:20 | 5:25 | 5:30 | 5:35 |
| pH | 4.95 | 4.94 | 4.94 | 4.88 | 4.86 | 4.85 | 4.85 |
已知:SO2能与水反应生成H2SO3,H2SO3不稳定,在空气中可被O2氧化成H2SO4.此外,在空气中,粉尘作催化剂,SO2还能被O2氧化成SO3,SO3也可与水反应生成H2SO4,H2SO4的酸性比H2SO3强。
①写出H2SO3与O2反应的化学方程式: 。
②在测定期间雨水的酸性 (填“增强”或“减弱”),其主要原因是 。
14.现有一包粗盐,其中含有少量氯化镁、硫酸钠和不溶性的泥沙。为获取纯净氯化钠,设计如图实验方案:
根据上述有关信息回答下列问题:
(1)滤渣1是 。
(2)向滤液1中加入过量NaOH溶液发生反应的化学方程式是 。
(3)滤液2中的溶质除NaCl外还有 (填化学式)。
(4)若④加入的盐酸不慎过量,对氯化钠的纯度 (填“有”或“无”)影响,理由是 。

| 阴离子阳离子 | OH﹣ | Cl﹣ | SO42﹣ | CO32﹣ |
| H+ | 溶、挥 | 溶 | 溶、挥 | |
| Na+ | 溶 | 溶 | 溶 | 溶 |
| Ba2+ | 溶 | 溶 | 不 | 不 |
| Mg2+ | 不 | 溶 | 溶 | 微 |
根据上述有关信息回答下列问题:
(1)滤渣1是 。
(2)向滤液1中加入过量NaOH溶液发生反应的化学方程式是 。
(3)滤液2中的溶质除NaCl外还有 (填化学式)。
(4)若④加入的盐酸不慎过量,对氯化钠的纯度 (填“有”或“无”)影响,理由是 。
15.某实验小组用KClO3和MnO2制取氧气,然后从制取后的残留固体中回收MnO2并用于实验室制取氯气(Cl2 )。部分实验装置如图所示。回答下列问题:

(1)写出装置Ⅰ中制取O2 的化学反应方程式: 。
(2)将制取氧气后的残留固体冷却、转移、 (填操作名称)、过滤、洗涤和干燥,即回收到MnO2.过滤装置Ⅱ中,仪器M的名称是 。
(3)将回收到的MnO2用于实验室制取Cl2.反应原理为:MnO2+4HCl(浓)
MnCl2+Cl2↑+2H2O,实验装置为Ⅲ和Ⅳ,实验时,将a口连接 (填“b”或“c”)口收集Cl2,收集到的Cl2中的杂质有 (填化学式)。
(4)洁厕灵(主要成分为盐酸)与“84”消毒液(主要成分为NaClO)混合也会反应生成Cl2:2HCl+NaClO═R+Cl2↑+H2O,生成物R的化学式为 。

(1)写出装置Ⅰ中制取O2 的化学反应方程式: 。
(2)将制取氧气后的残留固体冷却、转移、 (填操作名称)、过滤、洗涤和干燥,即回收到MnO2.过滤装置Ⅱ中,仪器M的名称是 。
(3)将回收到的MnO2用于实验室制取Cl2.反应原理为:MnO2+4HCl(浓)
| △ |
(4)洁厕灵(主要成分为盐酸)与“84”消毒液(主要成分为NaClO)混合也会反应生成Cl2:2HCl+NaClO═R+Cl2↑+H2O,生成物R的化学式为 。
16.浓硫酸与木炭在加热条件下可发生反应产生水和化学式为XO2型的气体。某化学课外兴趣小组的同学对XO2型气体的成分进行了实验探究。
【猜想】
(1)根据反应物组成元素及生成物的化学式类型,提出以下猜想:
【查阅资料】将SO2、CO2气体分别通入下列溶液中产生的有关现象如表:
【实验探究】
实验一:
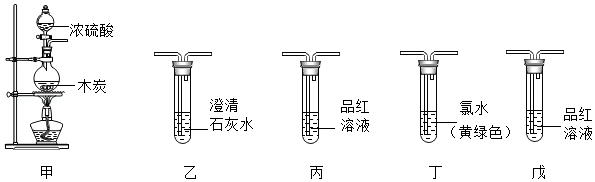
(2)将装置按甲→丙→(尾气处理)连接并进行实验。实验过程中观察到丙中溶液褪色,证明 不成立(填“猜想1”、“猜想2”或“猜想3”)。
实验二:
(3)将装置按甲→乙→(尾气处理)连接并进行实验。实验过程中观察到乙中澄清石灰水变浑浊。根据此现象能否确定CO2 的存在,理由是 。
实验三:
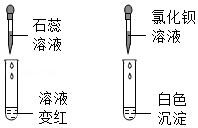
(4)将装置按甲→丙→丁→戊→乙→(尾气处理)连接并进行实验。实验过程中观察到丙、丁中溶液均褪色,戊中溶液颜色无变化,乙中澄清石灰水变浑浊。
①将反应后丁中溶液分成两等份分别置于两支试管中,并按如图所示操作进行实验。根据图中实验现象可判断反应后丁中溶液存在的离子有 。
②丁中溶液的作用是 。
【实验结论】
(5) (填“猜想1”、“猜想2”或“猜想3”)成立。
【问题讨论】
(6)在实验三中,若去掉装置戊,对实验结论 (填“有”或“无”)影响,理由是 。
【猜想】
(1)根据反应物组成元素及生成物的化学式类型,提出以下猜想:
| 猜想1 | 猜想2 | 猜想3 |
| 只有CO2 | 只有 | CO2和SO2都有 |
【查阅资料】将SO2、CO2气体分别通入下列溶液中产生的有关现象如表:
| 气体溶液 | SO2 | CO2 |
| 品红溶液 | 褪色 | 不褪色 |
| 氯水(黄绿色) | 褪色 | 不褪色 |
| 澄清石灰水 | 浑浊 | 浑浊 |
【实验探究】
实验一:

(2)将装置按甲→丙→(尾气处理)连接并进行实验。实验过程中观察到丙中溶液褪色,证明 不成立(填“猜想1”、“猜想2”或“猜想3”)。
实验二:
(3)将装置按甲→乙→(尾气处理)连接并进行实验。实验过程中观察到乙中澄清石灰水变浑浊。根据此现象能否确定CO2 的存在,理由是 。
实验三:

(4)将装置按甲→丙→丁→戊→乙→(尾气处理)连接并进行实验。实验过程中观察到丙、丁中溶液均褪色,戊中溶液颜色无变化,乙中澄清石灰水变浑浊。
①将反应后丁中溶液分成两等份分别置于两支试管中,并按如图所示操作进行实验。根据图中实验现象可判断反应后丁中溶液存在的离子有 。
②丁中溶液的作用是 。
【实验结论】
(5) (填“猜想1”、“猜想2”或“猜想3”)成立。
【问题讨论】
(6)在实验三中,若去掉装置戊,对实验结论 (填“有”或“无”)影响,理由是 。
17.实验室有一瓶久置的氢氧化钠固体,经检验只含有NaOH和Na2CO3两种物质。现取该固体样品12.5g溶于水配制成溶液。然后向溶液中滴加稀硫酸,同时收集反应产生的气体。当溶液中的溶质恰好全部转化成Na2SO4时,立即停止滴加稀硫酸。将产生的气体干燥后测定其质量为2.2g(假定溶液中无气体残留)。回答下列有关问题:
(1)写出碳酸钠与硫酸反应的化学方程式: 。
(2)氢氧化钠固体样品中NaOH的质量为 。
(3)计算所加稀硫酸的体积(稀硫酸的溶质质量分数为40%,密度为1.3g/cm3)。
[要求:第(3)小题写出计算过程且计算结果保留到小数点后1位]
(1)写出碳酸钠与硫酸反应的化学方程式: 。
(2)氢氧化钠固体样品中NaOH的质量为 。
(3)计算所加稀硫酸的体积(稀硫酸的溶质质量分数为40%,密度为1.3g/cm3)。
[要求:第(3)小题写出计算过程且计算结果保留到小数点后1位]
查看全部题目