下载高清试卷
【2020-2021学年河北省邢台市九年级(上)期中化学试卷】-第1页
试卷格式:2020-2021学年河北省邢台市九年级(上)期中化学试卷.PDF
试卷热词:最新试卷、2020年、河北试卷、邢台市试卷、化学试卷、九年级上学期试卷、期中试卷、初中试卷
扫码查看解析
试卷题目
1.下列变化属于化学变化的是( )
- A. 苹果榨汁
- B. 火药爆炸
- C. 空气液化
- D. 汽油挥发
2.下列做法中,不符合“低碳”理念的是( )
- A. 公交出行
- B. 浪费纸张
- C. 节约用电
- D. 道路绿化
3.每年5月31日为世界无烟日。吸烟有害健康,烟气中的一种有毒气体是( )
- A. O2
- B. N2
- C. CO
- D. CO2
4.下列实验操作中,正确的是( )
- A.
 CO2验满
CO2验满 - B.
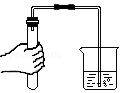 检查气密性
检查气密性 - C.
 滴加液体
滴加液体 - D.
 点燃酒精灯
点燃酒精灯
5.如图是空气成分示意图,其中R表示( )
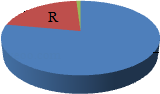

- A. 氮气
- B. 氧气
- C. 稀有气体
- D. 二氧化碳
6.日常生活中加碘食盐、高钙牛奶中的“碘”和“钙”指的是( )
- A. 单质
- B. 分子
- C. 原子
- D. 元素
7.下列用途中,主要利用物质化学性质的是( )
- A. 用石墨作电极
- B. 竹炭除冰箱中的异味
- C. 干冰用于人工降雨
- D. 食品包装袋中充入氮气
8.最早通过定量实验测定空气组成的科学家是( )
- A. 道尔顿
- B. 门捷列夫
- C. 拉瓦锡
- D. 阿伏加德罗
9.文房四宝“笔墨纸砚”中“墨”的主要成分是( )
- A. 碳
- B. 硅
- C. 磷
- D. 碘
10.下列气体中,都被计入空气污染指数项目的是( )
- A. 二氧化硫、二氧化氮、一氧化碳
- B. 二氧化硫、二氧化氮、氮气
- C. 二氧化硫、一氧化碳、氢气
- D. 二氧化碳、二氧化硫、臭氧
11.保持氧气化学性质的最小粒子是( )
- A. 氧元素
- B. 氧分子
- C. 氧原子
- D. 氧离子
12.下列化学符号或符号中“2”的含义表述正确的是( )
- A. 2H﹣﹣2个氢元素
- B. O2﹣﹣2个氧原子
- C. 2N2﹣﹣2个氮分子
- D. CO2﹣﹣二氧化碳中含有2个氧原子
13.下列实验方法能用于验证质量守恒定律的是( )
- A.

- B.
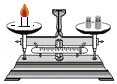
- C.

- D.

14.下列对实验现象的描述正确的是( )
- A. 硫在氧气中燃烧,产生淡蓝色火焰
- B. 红磷在空气中燃烧,产生大量白色烟雾
- C. 蜡烛在空气中燃烧,生成二氧化碳和水
- D. 铁丝在氧气中剧烈燃烧,火星四射,生成黑色固体
15.据报道,科学家发明了一种“月球制氧机”,这种“月球制氧机”可利用聚焦太阳能产生的高温加热月球土壤,制得氧气。据此可推测月球土壤中一定含有( )
- A. 氧化物
- B. 氧气
- C. 水
- D. 氧元素
16.硒元素具有抗衰老、抑制癌细胞生长的功能,其原子结构示意图及在元素周期表中的信息如图,下列说法错误的是( )


- A. 硒原子核内有34个质子
- B. 硒元素的相对原子质量是78.96g
- C. 硒元素位于元素周期表中第四周期
- D. 硒元素在某些化合物中可显﹣2价
17.下列与碳和碳的氧化物有关的说法中,正确的是( )
- A. 煤炉上放一盆水可防止CO中毒
- B. CO和CO2化学性质不同是因为分子构成不同
- C. CO2能使紫色石蕊溶液变红,说明CO2显酸性
- D. 用墨绘制的古画经久不变色,说明碳不与任何物质反应
18.我国科学家在纳米纸上“铺”一层“萘胺”(C10H9N)染料,制成一种试纸,用于检测食品中亚硝酸盐浓度的高低,下列说法正确的是( )
- A. 萘胺的相对分子质量为143g
- B. 萘胺中氮元素的质量分数最小
- C. 萘胺是由碳、氢、氮三种元素组成的
- D. 萘胺由10个碳原子、9个氢原子和1个氮原子构成
19.硅晶体广泛应用于电子工业的各个领域,工业上常用焦炭在高温下还原二氧化硅固体初步制得,主要反应为SiO2+2C
Si+2CO↑,下列说法不正确的是( )
| 高温 |
- A. 反应后固体质量减小
- B. 此反应中SiO2被还原
- C. SiO2中硅元素的化合价为+4
- D. 地壳中硅元素含量小于铁元素
20.甲和乙在一定条件下反应生成丙和丁,微观示意图如图。有关说法正确的是( )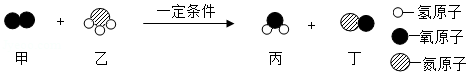

- A. 反应前后分子的种类、数目均不变
- B. 反应前后各元素的化合价均不变
- C. 参加反应的甲和乙分子个数比为5:4
- D. 丙物质由2个氢原子和1个氧原子构成
21.四种物质在一定条件下充分反应,测得反应前后各物质的质量分数如图所示,下列说法不正确的是( )
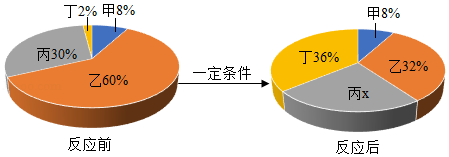

- A. 该反应是化合反应
- B. 反应后x的数值为24%
- C. 甲物质可能是该反应的催化剂
- D. 反应中乙与丁的质量变化之比为8:9
22.用如图所示4个实验探究二氧化碳能否与水反应(实验中所用的纸花均用石蕊染成紫色并干燥),下列说法正确的是( )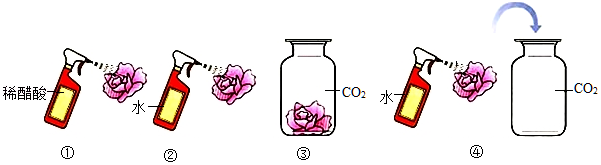
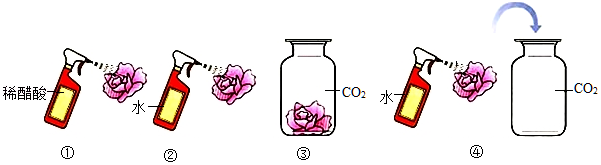
- A. 最终只有实验④中的紫色石蕊小花会变红
- B. 实验④就能说明二氧化碳与水发生了反应
- C. 由实验①④推断,实验④中有酸性物质生成
- D. 在实验④中,若对比小花放入集气瓶前后的现象,可以不必做实验③
23.下列探究实验能达到实验目的的是( )
- A. 探究温度对分子运动速率的影响,只将少量品红加入到热水中
- B. 探究空气中氧气的含量,用铁丝代替红磷在空气中燃烧进行实验
- C. 探究MnO2是否是H2O2分解的催化剂,比较MnO2加到H2O2溶液前后产生气泡快慢
- D. 探究吸入空气和呼出气体中O2含量不同,将燃着的木条分别伸入等体积两种气体中
24.生活中的化学知识随处可见。

(1)医疗急救常用到纯氧,这利用了氧气的性质是 。
(2)碳酸饮料中的碳酸化学式是 。
(3)如图是某品牌矿泉水的部分标签内容,其中钠离子的符号是 。
(4)“84消毒液”的主要成分是次氯酸钠(NaClO)。其中氯元素的化合价是 。制取NaClO的原理是2NaOH+Cl2═NaClO+X+H2O,其中X的化学式是 。
(5)把磨好的豆浆倒在纱布袋中将渣和浆分离,相当于化学实验中的 操作。

(1)医疗急救常用到纯氧,这利用了氧气的性质是 。
(2)碳酸饮料中的碳酸化学式是 。
(3)如图是某品牌矿泉水的部分标签内容,其中钠离子的符号是 。
(4)“84消毒液”的主要成分是次氯酸钠(NaClO)。其中氯元素的化合价是 。制取NaClO的原理是2NaOH+Cl2═NaClO+X+H2O,其中X的化学式是 。
(5)把磨好的豆浆倒在纱布袋中将渣和浆分离,相当于化学实验中的 操作。
25.请结合水的有关知识回答。
(1)自然界中的水属于 (填“纯净物”或“混合物”)。
(2)为区分软水和硬水,将等量的肥皂水分别滴加到盛有等量软水、硬水的试管中,振荡,试管中产生较多泡沫的为 。生活上常用 的方法来降低水的硬度。
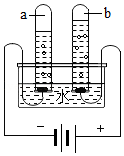
(3)如图是电解水的实验示意图,试管 (填“a”或“b”)中的气体能使燃着的木条燃烧更旺,试管a、b中产生气体的体积比约为 ,电解水反应的符号表达式为 ,该反应前后不变的粒子是 (填“分子”或“原子”)。
(4)净化水的操作有①过滤②蒸馏③静置沉淀等多种。其中净化程度最高的操作是 (填序号),净水器中经常使用活性炭,主要是利用活性炭的 性。
(5)爱护水资源,人人有责。请写出一条节约用水的措施 。

(1)自然界中的水属于 (填“纯净物”或“混合物”)。
(2)为区分软水和硬水,将等量的肥皂水分别滴加到盛有等量软水、硬水的试管中,振荡,试管中产生较多泡沫的为 。生活上常用 的方法来降低水的硬度。
(3)如图是电解水的实验示意图,试管 (填“a”或“b”)中的气体能使燃着的木条燃烧更旺,试管a、b中产生气体的体积比约为 ,电解水反应的符号表达式为 ,该反应前后不变的粒子是 (填“分子”或“原子”)。
(4)净化水的操作有①过滤②蒸馏③静置沉淀等多种。其中净化程度最高的操作是 (填序号),净水器中经常使用活性炭,主要是利用活性炭的 性。
(5)爱护水资源,人人有责。请写出一条节约用水的措施 。
26.元素周期表是学习化学的重要工具,如表为元素周期表中部分元素的相关信息,利用如表回答相关问题。
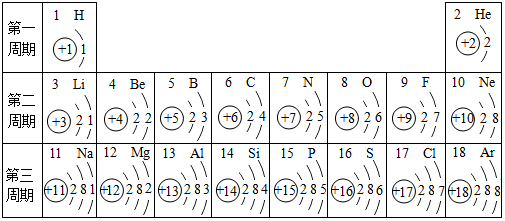
(1)原子序数为4的元素符号为 。
(2)C、N、O排在同一周期是因为 (填“质子数”“电子层数”或“最外层电子数”)相同。
(3)He和Mg的化学性质 (填“相似”或“不相似”)。
(4)钠离子核外电子排布与 (填元素符号)原子核外电子排布相同。
(5)一个磷原子含有 个质子,一个NH4+含有 个电子。
(6)由第12号元素与第17号元素组成化合物的化学式为 。

(1)原子序数为4的元素符号为 。
(2)C、N、O排在同一周期是因为 (填“质子数”“电子层数”或“最外层电子数”)相同。
(3)He和Mg的化学性质 (填“相似”或“不相似”)。
(4)钠离子核外电子排布与 (填元素符号)原子核外电子排布相同。
(5)一个磷原子含有 个质子,一个NH4+含有 个电子。
(6)由第12号元素与第17号元素组成化合物的化学式为 。
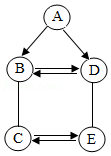
27.A~E是初中化学常见的物质,它们之间的转化关系如图所示。其中A、B是两种组成元素相同的液体,C、E是两种组成元素相同的气体,(部分反应条件、反应物及生成物已略去)
请回答下列问题:
(1)A物质的化学式为 。
(2)E物质的一种用途为 。
(3)D与E发生的反应属于最基本的反应类型 。
(4)C生成E反应的化学方程式为 。

请回答下列问题:
(1)A物质的化学式为 。
(2)E物质的一种用途为 。
(3)D与E发生的反应属于最基本的反应类型 。
(4)C生成E反应的化学方程式为 。
28.请结合下列实验装置,回答问题: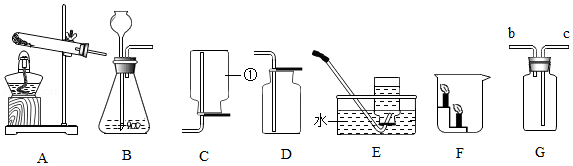
(1)写出标号①仪器的名称 。
(2)写出实验室用高锰酸钾制取氧气的化学方程式 ,可选择装置 (填字母序号)作为气体发生装置,但在该装置中还需要补充的是 。实验室要得到比较纯净的氧气通常选用 (填字母序号)装置收集。
(3)实验室常用大理石和稀盐酸制取二氧化碳气体,收集气体应选用装置 (从装置A~E选择填序号);若将收集到的二氧化碳气体,沿烧杯内壁慢慢倒入装置F中,可以观察到的现象是 ,说明二氧化碳具有 的物理性质。
(4)若要用G装置检验CO2,在G装置中盛放的试剂名称是 ,CO2应从 (填“b”或“c”)端通入,实验现象为 ,反应的化学方程式为 。

(1)写出标号①仪器的名称 。
(2)写出实验室用高锰酸钾制取氧气的化学方程式 ,可选择装置 (填字母序号)作为气体发生装置,但在该装置中还需要补充的是 。实验室要得到比较纯净的氧气通常选用 (填字母序号)装置收集。
(3)实验室常用大理石和稀盐酸制取二氧化碳气体,收集气体应选用装置 (从装置A~E选择填序号);若将收集到的二氧化碳气体,沿烧杯内壁慢慢倒入装置F中,可以观察到的现象是 ,说明二氧化碳具有 的物理性质。
(4)若要用G装置检验CO2,在G装置中盛放的试剂名称是 ,CO2应从 (填“b”或“c”)端通入,实验现象为 ,反应的化学方程式为 。
29.兴趣小组同学发现在做木炭还原氧化铜的实验时,较难得到纯净的铜,为此进行了如下探究:
【提出问题】影响碳还原氧化铜的实验条件有哪些?
【猜想与假设】(1)加热方式(试管的角度);(2)木炭粉和氧化铜的质量比。
【查阅资料】碳还原氧化铜得到的铜中可能含有少量的氧化亚铜;铜不能与稀硫酸反应。氧化亚铜为红色固体,能与稀硫酸反应:Cu2O+H2SO4═CuSO4+H2O+Cu。
【进行实验】
实验1:取质量比1:11的木炭粉和氧化铜混合物1.3g,进行实验。
【问题与解释】
(1)木炭粉和氧化铜反应的化学方程式为 。
(2)该实验的探究目的是 。
(3)酒精灯加金属网的目的是 。
实验2:取一定量的混合物,用1﹣2装置进行实验。
【解释与结论】实验2的结论是 。
【反思与评价】
(1)实验2没有进行质量比为1:14的实验,理由是 。
(2)为检验2﹣4的红色固体中是否含Cu2O,所需试剂是 。
【提出问题】影响碳还原氧化铜的实验条件有哪些?
【猜想与假设】(1)加热方式(试管的角度);(2)木炭粉和氧化铜的质量比。
【查阅资料】碳还原氧化铜得到的铜中可能含有少量的氧化亚铜;铜不能与稀硫酸反应。氧化亚铜为红色固体,能与稀硫酸反应:Cu2O+H2SO4═CuSO4+H2O+Cu。
【进行实验】
实验1:取质量比1:11的木炭粉和氧化铜混合物1.3g,进行实验。
| 序号 | 1﹣1 | 1﹣2 |
| 装置 |  | 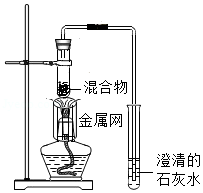 |
| 反应后物质的颜色、状态 | 黑色粉末中混有少量红色固体 | 红色固体有金属光泽,混有极少量黑色物质 |
【问题与解释】
(1)木炭粉和氧化铜反应的化学方程式为 。
(2)该实验的探究目的是 。
(3)酒精灯加金属网的目的是 。
实验2:取一定量的混合物,用1﹣2装置进行实验。
| 序号 | 木炭粉与氧化铜的质量比 | 反应后物质的颜色、状态 | |
| 2﹣1 | 1:9 | 红色固体有金属光泽 | 混有少量黑色物质 |
| 2﹣2 | 1:10 | 混有很少量黑色物质 | |
| 2﹣3 | 1:11 | 混有极少量黑色物质 | |
| 2﹣4 | 1:12 | 无黑色物质 | |
| 2﹣5 | 1:13 | 混有较多黑色物质 | |
【解释与结论】实验2的结论是 。
【反思与评价】
(1)实验2没有进行质量比为1:14的实验,理由是 。
(2)为检验2﹣4的红色固体中是否含Cu2O,所需试剂是 。
30.为测定某石灰石样品中碳酸钙的质量分数,兴趣小组进行了如图实验(杂质不参加反应也不溶于水)。请计算:
(1)生成二氧化碳 g;
(2)求石灰石样品中碳酸钙的质量分数。

(1)生成二氧化碳 g;
(2)求石灰石样品中碳酸钙的质量分数。

查看全部题目
相关试卷推荐
更多热门试卷
如何查看答案以及解析
扫描右侧二维码查看试卷答案解析以及视频讲解