下载高清试卷
【2021-2022学年山东省威海市经开区九年级(上)期中化学试卷】-第1页
试卷格式:2021-2022学年山东省威海市经开区九年级(上)期中化学试卷.PDF
试卷热词:最新试卷、2021年、山东试卷、威海市试卷、化学试卷、九年级上学期试卷、期中试卷、初中试卷

扫码查看解析
试卷题目
1.分类法是化学学习的重要方法之一,下列各组物质按照单质、盐、混合物的顺序排列的是( )
- A. 生铁、氢氧化铜、冰水混合物
- B. 液氧、硫酸钡、粗盐
- C. 天然气、纯碱、石油
- D. 钙片、氯化镁、海水
2.实验室许多药品需要密封保存,下列药品都需密封保存,其原因解释错误的是( )
- A. 浓盐酸-防止挥发
- B. 生石灰-防止与氧气反应
- C. 浓硫酸-防止吸水
- D. NaOH溶液-防止与CO2反应
3.将一定质量的饱和氯化钠溶液通电一段时间后,下列叙述不正确的是(反应原理为:2NaCl+2H2O═2NaOH+H2↑+Cl2↑)( )
- A. 溶液的pH逐渐增大
- B. 氯化钠溶液的溶质质量减小
- C. 溶液中氧元素的质量不变
- D. 溶液中钠元素的质量分数变小
4.浩瀚无际的海洋为人类提供了丰富的资源,下列有关海洋资源的叙述错误的是( )
- A. 利用多级闪急蒸馏法可淡化海水
- B. 利用锰结核可获取多种金属
- C. 利用向海水中加入石灰乳的方法可以将海水中的Mg2+富集沉淀出来
- D. 利用海底蕴藏的大量“可燃冰”作燃料,不会加剧温室效应
5.配制130g溶质质量分数为6%的氯化钠溶液时,下列操作会导致结果偏大的是( )
①称量的氯化钠固体中含有不溶性杂质;
②用量筒量取水时俯视读数:
③将氯化钠固体放在托盘天平的右盘称量;
④往烧杯中加水时有水洒出;
⑤转移配好的溶液时有少量溅出。
①称量的氯化钠固体中含有不溶性杂质;
②用量筒量取水时俯视读数:
③将氯化钠固体放在托盘天平的右盘称量;
④往烧杯中加水时有水洒出;
⑤转移配好的溶液时有少量溅出。
- A. ②③
- B. ①④
- C. ②④
- D. ③⑤
6.逻辑推理是化学学习常用的思维方法,下列推理正确的是( )
- A. 饱和溶液不能继续溶解某溶质,则饱和溶液也不能继续溶解其他溶质
- B. 中和反应有盐和水生成,因此有盐和水生成的反应一定是中和反应
- C. 溶液中有晶体析出时,溶质质量减小,所以溶质的质量分数一定减小
- D. 酸性溶液能使石蕊试液变红色,所以能使石蕊试液变红的溶液一定是酸性溶液
7.下列实验操作或对意外事故的处理不正确的是( )
- A. 烧碱溶液不小心沾到皮肤上要立即用大量的水冲洗,再涂上硼酸溶液
- B. 稀释浓硫酸时将水沿着器壁慢慢注入浓硫酸中,并用玻璃棒不断的搅拌
- C. 酒精灯洒出的酒精在桌上燃烧,立即用湿布或沙子扑灭
- D. 浓硫酸沾到皮肤上,立即用大量的水冲洗,再涂上3%-5%的碳酸氢钠溶液
8.物质的鉴别和除杂是重要的实验技能。下列实验方法不能达到实验目的的是( )
| 选项 | 实验目的 | 实验方法 |
| A | 检验久置的NaOH是否变质 | 取少量样品,加水充分溶解,滴加CaCl2溶液 |
| B | 鉴别NaOH和NH4NO3两种固体 | 取少量样品,加水充分溶解,触摸烧杯外壁 |
| C | 分离CaO与CaCO3固体混合物 | 加水充分溶解后,过滤 |
| D | 除去CaCl2溶液中混有盐酸 | 加入过量的CaCO3,过滤 |
- A. A
- B. B
- C. C
- D. D
9.如图是A、B、C三种固体物质的溶解度曲线图,下列说法错误的是( )
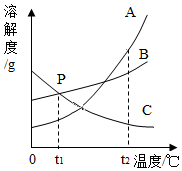

- A. t2℃时,A、B、C三种物质中,A物质的溶解度最大
- B. P点表示t1℃时B、C两溶液的溶质质量分数相等
- C. t2℃时,给等质量的A、B、C三种物质的饱和溶液,分别降温到t1℃,析出晶体最多的是A物质
- D. 从A、B的混合物中提纯A,应采用降温结晶法
10.下列宏观现象的微观解释,不正确的是( )
- A. 含有酚酞的烧碱溶液中加入稀硫酸,红色消失-----氢离子与氢氧根离子结合成水分子
- B. 水银温度计放入热水中,水银柱升高-----原子体积受热变大
- C. 一氧化碳有毒,二氧化碳无毒------不同种分子化学性质不同
- D. 硝酸银溶液中滴入氯化钠溶液,产生沉淀-----银离子与氯离子结合成难溶性氯化银
11.研究物质的溶解对于生产、生活有着重要意义。
下表是碳酸钠的部分溶解度数据。
(1)由表中数据可知,碳酸钠属于 物质(填“易溶”“可溶”“微溶”或“难溶”)。
(2)由表中数据可知,碳酸钠的溶解度随温度升高 。
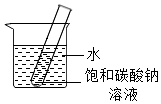
(3)小东同学进行了如图所示的实验,若使烧杯③中的溶液达到饱和,至少需再加入 g碳酸钠;升温至60℃时,烧杯④中会出现的现象是 。

(4)20℃时,将装有饱和碳酸钠溶液(底部有碳酸钠粉末)的小试管放入盛水的烧杯中(如图)。向烧杯中加入某物质后,试管底部的粉末减少,则加入的物质可能是 (填字母序号),该物质形成的溶液中存在的微粒有 。
A.氢氧化钠
B.碳酸钙
C.硝酸铵
D.氯化钠
下表是碳酸钠的部分溶解度数据。
| 温度/℃ | 20 | 30 | 40 | 50 | 60 | 80 | 100 |
| 溶解度/g | 21.8 | 39.7 | 48.8 | 47.3 | 46.4 | 45.1 | 44.7 |
(1)由表中数据可知,碳酸钠属于 物质(填“易溶”“可溶”“微溶”或“难溶”)。
(2)由表中数据可知,碳酸钠的溶解度随温度升高 。
(3)小东同学进行了如图所示的实验,若使烧杯③中的溶液达到饱和,至少需再加入 g碳酸钠;升温至60℃时,烧杯④中会出现的现象是 。

(4)20℃时,将装有饱和碳酸钠溶液(底部有碳酸钠粉末)的小试管放入盛水的烧杯中(如图)。向烧杯中加入某物质后,试管底部的粉末减少,则加入的物质可能是 (填字母序号),该物质形成的溶液中存在的微粒有 。

A.氢氧化钠
B.碳酸钙
C.硝酸铵
D.氯化钠
12.只用H、C、O、Cl、Ca、Na六种元素中的一种或几种组成符合要求的物质,完成填空:
(1)
只用上述元素中的一种或几种组成符合要求的物质,完成下列化学方程式:
(2)中和反应 ,微观实质 。
(3)有气体生成的复分解反应 。
(1)
| 物质组成(化学式) | 构成物质的粒子(用符号表示) | 物质的类别 | |
| 1、导致露置空气中的烧碱变质的物质 | |||
| 2、常用于改良酸性土壤的物质 | |||
| 3、氢氧化钠完全变质后的物质 | |||
| 4、可做食品干燥剂的物质 |
只用上述元素中的一种或几种组成符合要求的物质,完成下列化学方程式:
(2)中和反应 ,微观实质 。
(3)有气体生成的复分解反应 。
13.构建知识网络模型是化学学习中重要的学习方法。如图1是小明同学利用左手构建的酸的化学性质知识网络。
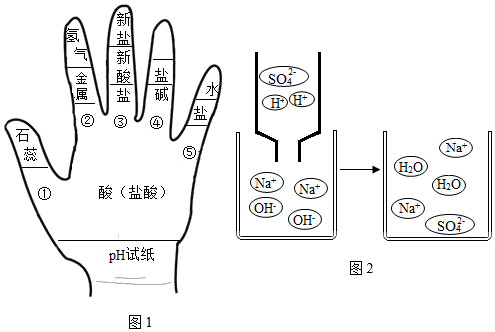
请完成下列问题:
(1)如用湿润的pH试纸测定盐酸的pH,则结果会 (填“偏大”“偏小”或“无影响”)。
(2)图1中①的现象是 。
(3)世界卫生组织推广使用中国铁锅,使用铁锅炒菜时,放点食醋可以补充人体中构成血红素Fe元素,该反应的原理是利用了酸的化学性质,该变化过程中相互作用的微粒为 ,微粒转化过程 。
(4)小明用图2来说明稀硫酸与氢氧化钠溶液反应的过程,该过程不发生变化的微粒是 (用符号表示),该反应的微观实质可表示为H++OH-═H2O,依此类推当图1中③是向稀盐酸中滴加硝酸银溶液时,反应的微观实质用同样的方法可表示为 。
(5)图1中⑤的性质可用于除铁锈,反应的化学方程式为 。
(6)盐酸、硫酸、食醋具有相似化学性质的原因 。

请完成下列问题:
(1)如用湿润的pH试纸测定盐酸的pH,则结果会 (填“偏大”“偏小”或“无影响”)。
(2)图1中①的现象是 。
(3)世界卫生组织推广使用中国铁锅,使用铁锅炒菜时,放点食醋可以补充人体中构成血红素Fe元素,该反应的原理是利用了酸的化学性质,该变化过程中相互作用的微粒为 ,微粒转化过程 。
(4)小明用图2来说明稀硫酸与氢氧化钠溶液反应的过程,该过程不发生变化的微粒是 (用符号表示),该反应的微观实质可表示为H++OH-═H2O,依此类推当图1中③是向稀盐酸中滴加硝酸银溶液时,反应的微观实质用同样的方法可表示为 。
(5)图1中⑤的性质可用于除铁锈,反应的化学方程式为 。
(6)盐酸、硫酸、食醋具有相似化学性质的原因 。
14.2021年6月8日是第13个“世界海洋日”,威海有漫长的海岸线,蕴藏着丰富的海洋资源。某兴趣小组设计的综合利用海水的部分流程图如图,据图回答:
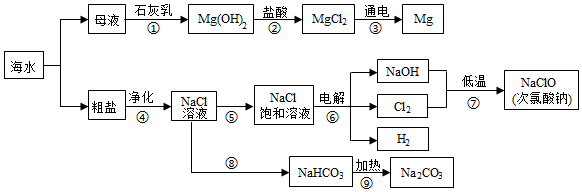
(1)海水制镁。步骤①②③是利用母液制镁的流程,该流程中发生中和反应的化学方程式是 。步骤①中制取氢氧化镁选择向母液中加入石灰乳,而不是向海水中直接加入石灰乳,原因是 。
(2)海水晒盐。通常采用 (填“降温”或“蒸发”)结晶的方法使海水中的氯化钠析出,通过步骤④除去粗盐溶液中含有的MgCl2、Na2SO4、CaCl2等可溶性杂质,需要依次加入过量的 溶液,然后过滤,在滤液中加入适量的稀盐酸,其中过滤操作需要的玻璃仪器有 。
(3)海水制碱。步骤⑧⑨是氨碱法制纯碱的流程,步骤⑧先向饱和食盐水中通入氨气,再通入二氧化碳,这样做的目的是 ,步骤⑧⑨中发生反应的化学方程式是 。
(4)我国化学家侯德榜创立的联合制碱法的优点有 。
A.无“索尔维氨碱法”中的废弃物CaCl2生成,有利于保护环境
B.大大提高了食盐的利用率
C.将“制碱”与制氨生产联合起来,同时析出的NH4Cl晶体可用作氮肥
(5)步骤⑥是电解NaCl饱和溶液制取烧碱,该反应中的反应物是 。
(6)步骤⑦用烧碱低温制取次氯酸钠的反应原理为:Cl2+2NaOH═X+NaClO+H2O。则X的化学式是 。

(1)海水制镁。步骤①②③是利用母液制镁的流程,该流程中发生中和反应的化学方程式是 。步骤①中制取氢氧化镁选择向母液中加入石灰乳,而不是向海水中直接加入石灰乳,原因是 。
(2)海水晒盐。通常采用 (填“降温”或“蒸发”)结晶的方法使海水中的氯化钠析出,通过步骤④除去粗盐溶液中含有的MgCl2、Na2SO4、CaCl2等可溶性杂质,需要依次加入过量的 溶液,然后过滤,在滤液中加入适量的稀盐酸,其中过滤操作需要的玻璃仪器有 。
(3)海水制碱。步骤⑧⑨是氨碱法制纯碱的流程,步骤⑧先向饱和食盐水中通入氨气,再通入二氧化碳,这样做的目的是 ,步骤⑧⑨中发生反应的化学方程式是 。
(4)我国化学家侯德榜创立的联合制碱法的优点有 。
A.无“索尔维氨碱法”中的废弃物CaCl2生成,有利于保护环境
B.大大提高了食盐的利用率
C.将“制碱”与制氨生产联合起来,同时析出的NH4Cl晶体可用作氮肥
(5)步骤⑥是电解NaCl饱和溶液制取烧碱,该反应中的反应物是 。
(6)步骤⑦用烧碱低温制取次氯酸钠的反应原理为:Cl2+2NaOH═X+NaClO+H2O。则X的化学式是 。
15.某兴趣小组进行粗盐(杂质只含有泥沙)提纯实验,并利用所得精盐配制100g溶质质量分数为15%的氯化钠溶液。请完成下列问题:
实验一:如图是甲同学进行粗盐提纯实验的操作示意图。
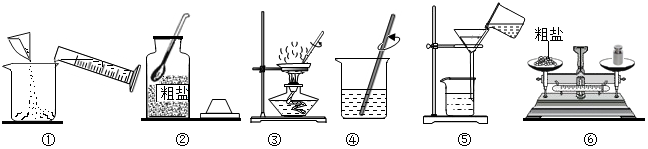
(1)进行操作③时,当观察到 时,停止加热。
(2)操作④中玻璃棒的作用是 。
(3)操作⑤中有一处明显的错误,请你帮他们指出来 。图中错误改正后,粗盐提纯实验的正确操作顺序为 (填操作示意图的序号)。
实验二:乙同学用提纯得到的精盐配制100g溶质质量分数为15%的氯化钠溶液(假设称量氯化钠时1g以下用游码)。
(4)配制时,除图中提供的仪器外,还需要试剂瓶、镊子和 (填一种仪器名称)。
(5)称量氯化钠时如果发现指针偏向右侧,正确的操作是 ,如果称量时氯化钠和砝码位置颠倒了,其它操作步骤均正确,则所配制溶液的溶质质量分数 (填“大于”“等于”或“小于”)15%。
(6)量水时应选择量筒的规格是 mL(填“10”“50”或“100”)。
【反思拓展】
(7)经检测所配溶液的溶质质量分数偏小,原因可能是 (列举一条即可)。
(8)海水晒盐采用操作③的原理而不用冷却氯化钠热饱和溶液的方法,原因是 。
实验一:如图是甲同学进行粗盐提纯实验的操作示意图。

(1)进行操作③时,当观察到 时,停止加热。
(2)操作④中玻璃棒的作用是 。
(3)操作⑤中有一处明显的错误,请你帮他们指出来 。图中错误改正后,粗盐提纯实验的正确操作顺序为 (填操作示意图的序号)。
实验二:乙同学用提纯得到的精盐配制100g溶质质量分数为15%的氯化钠溶液(假设称量氯化钠时1g以下用游码)。
(4)配制时,除图中提供的仪器外,还需要试剂瓶、镊子和 (填一种仪器名称)。
(5)称量氯化钠时如果发现指针偏向右侧,正确的操作是 ,如果称量时氯化钠和砝码位置颠倒了,其它操作步骤均正确,则所配制溶液的溶质质量分数 (填“大于”“等于”或“小于”)15%。
(6)量水时应选择量筒的规格是 mL(填“10”“50”或“100”)。
【反思拓展】
(7)经检测所配溶液的溶质质量分数偏小,原因可能是 (列举一条即可)。
(8)海水晒盐采用操作③的原理而不用冷却氯化钠热饱和溶液的方法,原因是 。
16.某化学课堂围绕“酸碱中和反应”,在老师引导下开展探究活动。
资料:①KOH与NaOH化学性质相似;②K2CO3与Na2CO3化学性质相似。
【演示实验】氢氧化钾溶液与稀硫酸混合,直接观察不到明显现象,为证明氢氧化钾溶液与稀硫酸发生了反应,三位同学进行了以下实验。
(1)测定溶液pH的方法
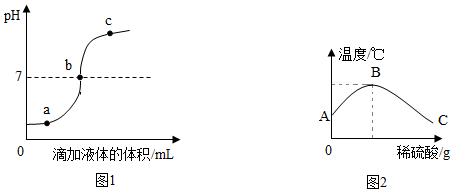
小红同学在实验过程中用pH试纸测的pH变化如图1所示,小红是将 溶液滴向 溶液中,证明发生了化学反应的依据是 ,反应的化学方程式 ,为C点的阴离子有 。
(2)测混合过程中的温度变化
由图2知,稀硫酸与氢氧化钾溶液发生的反应是放热反应。
①B点表示的含义是 。
②C点溶质 。
(3)借助于酸碱指示剂
小明同学通过图3所示实验,他观察到溶液由红色变成无色,也证明氢氧化钾溶液与稀硫酸发生了化学反应。小明同学继续探究:反应后溶液中溶质是什么呢?针对疑问,大家纷纷提出猜想。

猜想一:只有K2SO4
猜想二:有K2SO4和H2SO4
猜想三:有K2SO4和H2SO4和KOH
其他同学认为有一种猜想是不合理的,理由是 。
(4)为了验证其余猜想,各学习小组选用BaCl2溶液、生锈铁钉,进行如下方案的探究:
(5)小芳针对上述方案提出疑问,有一个方案是不合理的,理由是 。
(6)(反思交流)小花向氢氧化钾溶液中滴加稀硫酸,看到了气泡,她很想知道这瓶氢氧化钾溶液的成分,你能帮她设计实验方案吗?方案: 。(请写出操作、现象、结论)
资料:①KOH与NaOH化学性质相似;②K2CO3与Na2CO3化学性质相似。
【演示实验】氢氧化钾溶液与稀硫酸混合,直接观察不到明显现象,为证明氢氧化钾溶液与稀硫酸发生了反应,三位同学进行了以下实验。
(1)测定溶液pH的方法

小红同学在实验过程中用pH试纸测的pH变化如图1所示,小红是将 溶液滴向 溶液中,证明发生了化学反应的依据是 ,反应的化学方程式 ,为C点的阴离子有 。
(2)测混合过程中的温度变化
由图2知,稀硫酸与氢氧化钾溶液发生的反应是放热反应。
①B点表示的含义是 。
②C点溶质 。
(3)借助于酸碱指示剂
小明同学通过图3所示实验,他观察到溶液由红色变成无色,也证明氢氧化钾溶液与稀硫酸发生了化学反应。小明同学继续探究:反应后溶液中溶质是什么呢?针对疑问,大家纷纷提出猜想。

猜想一:只有K2SO4
猜想二:有K2SO4和H2SO4
猜想三:有K2SO4和H2SO4和KOH
其他同学认为有一种猜想是不合理的,理由是 。
(4)为了验证其余猜想,各学习小组选用BaCl2溶液、生锈铁钉,进行如下方案的探究:
| 实验方案 | 加入生锈铁钉 | 滴加BaCl2溶液 |
| 实验现象 | 产生白色沉淀 | |
| 实验结论 | 溶液中有H2SO4 相关化学方程式 | 溶液中有H2SO4 |
(5)小芳针对上述方案提出疑问,有一个方案是不合理的,理由是 。
(6)(反思交流)小花向氢氧化钾溶液中滴加稀硫酸,看到了气泡,她很想知道这瓶氢氧化钾溶液的成分,你能帮她设计实验方案吗?方案: 。(请写出操作、现象、结论)
17.为测定某盐酸的溶质质量分数,取200g样品于烧杯中,将50g碳酸钠溶液分为5等份,分5次加入盛有样品的烧杯中。测出每次反应后溶液的总质量,实验数据如下表:
请根据实验数据计算盐酸的溶质质量分数。
| 第一次 | 第二次 | 第三次 | 第四次 | 第五次 | |
| 加入Na2CO3溶液的质量 | 10g | 10g | 10g | 10g | 10g |
| 反应后溶液的质量 | 208.9g | 217.8g | 226.7g | 235.6g | 245.6g |
请根据实验数据计算盐酸的溶质质量分数。
查看全部题目
相关试卷推荐
更多热门试卷
如何查看答案以及解析
扫描右侧二维码查看试卷答案解析以及视频讲解