下载高清试卷
【2018年吉林省中考化学试卷】-第1页
试卷格式:2018年吉林省中考化学试卷.PDF
试卷热词:最新试卷、2018年、吉林试卷、化学试卷、九年级试卷、中考试卷、初中试卷
扫码查看解析
试卷题目
1.物质的下列性质中,属于化学性质的是( )
- A. 可燃性
- B. 状态
- C. 气味
- D. 硬度
2.空气是一种宝贵的资源,空气中体积分数最大的气体是( )
- A. 稀有气体
- B. 二氧化碳
- C. 氧气
- D. 氮气
3.生活中可以使硬水软化成软水的常用方法是( )
- A. 沉降
- B. 消毒
- C. 煮沸
- D. 过滤
4.下列实验操作正确的是( )
- A.
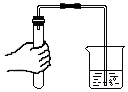 检查装置气密性
检查装置气密性 - B.
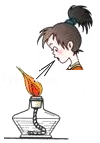 熄灭酒精灯
熄灭酒精灯 - C.
 量取液体
量取液体 - D.
 移走蒸发皿
移走蒸发皿
5.有关物质的用途,错误的是( )
- A. 石墨做电极
- B. 干冰用于人工降雨
- C. NH4Cl当做复合肥使用
- D. 小苏打用于焙制糕点
6.化学方程式____+3CO
2Fe+3CO2中,所缺物质的化学式为( )
| 高温 |
- A. FeO
- B. Fe2O3
- C. Fe3O4
- D. FeCO3
7."保护好我们的环境"是每位公民应尽的义务。下列说法正确的是( )
- A. 农药本身有毒,应该禁止施用农药
- B. 有害气体和烟尘会对空气造成污染
- C. 煤燃烧产生的二氧化碳会造成酸雨
- D. 工业废水不经处理就可以排放到江河里
8.关于电解水实验的下列说法中正确的是( )
- A. 从现象上判断:正极产生的是氢气
- B. 从变化上分类:该变化属于物理变化
- C. 从宏观上分析:水是由氢气和氧气组成的
- D. 从微观上分析:水分子是由氢原子和氧原子构成的
9.下列实验设计能够实现其对应实验目的是( )
- A.
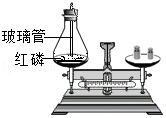 验证质量守恒定律
验证质量守恒定律 - B.
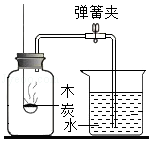 测定空气中氧气含量
测定空气中氧气含量 - C.
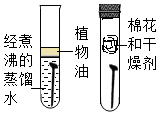 探究铁钉锈蚀的条件
探究铁钉锈蚀的条件 - D.
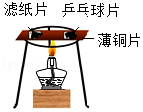 探究燃烧条件之一:温度达到着火点
探究燃烧条件之一:温度达到着火点
10.下列实验方案正确的是( )
- A. 制备:用加热KCl和MnO2混合物的方法制O2
- B. 鉴别:用稀盐酸鉴别铁粉、木炭粉和氧化铜粉末
- C. 除杂:用溶解、蒸发的方法除去粗盐中的难溶性杂质
- D. 检验:用内壁涂有澄清石灰水的烧杯罩在甲烷燃烧的火焰上方,检验有水生成
11.高纯硅是制造"芯片"的重要材料。根据图回答下列问题。
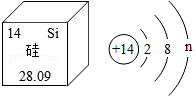
(1)硅原子的相对原子质量是 ;
(2)硅原子的最外层电子数n= ;
(3)沙子的主要成分是SiO2,SiO2中硅元素的化合价为 价。

(1)硅原子的相对原子质量是 ;
(2)硅原子的最外层电子数n= ;
(3)沙子的主要成分是SiO2,SiO2中硅元素的化合价为 价。
12.请完成下列思维导图。
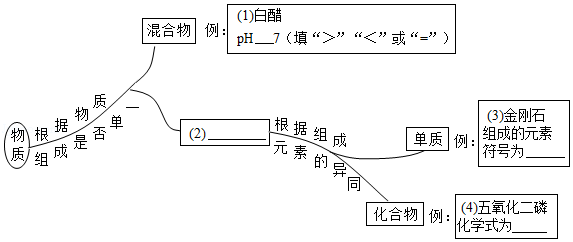

13.某学校学生的午餐为米饭、炖牛肉、炒芹菜、油炸花生米等;餐具为竹制筷子、塑料饭盒。
(1)午餐中的牛肉富含的营养素是 ;
(2)用有机合成材料制成的餐具是 ;
(3)午餐后用洗涤剂清洗餐具上的油污,是利用了 原理。
(1)午餐中的牛肉富含的营养素是 ;
(2)用有机合成材料制成的餐具是 ;
(3)午餐后用洗涤剂清洗餐具上的油污,是利用了 原理。
14.物质的变化常伴随能量变化。
(1)能量的变化常表现为温度的改变。稀释浓硫酸时,溶液的温度 ;
(2)氢气被认为是理想的清洁、高能燃料。请写出氢气在氧气中燃烧的化学方程式 。
(1)能量的变化常表现为温度的改变。稀释浓硫酸时,溶液的温度 ;
(2)氢气被认为是理想的清洁、高能燃料。请写出氢气在氧气中燃烧的化学方程式 。
15.根据如图中甲、乙两种固体物质的溶解度曲线回答问题。
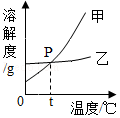
(1)P点的含义:在t℃时甲与乙的溶解度 ;
(2)在温度不变的情况下,把乙的不饱和容液变为饱和溶液的方法是 ;
(3)甲中含有少量的乙,若提纯甲应采用的结晶方法是 。

(1)P点的含义:在t℃时甲与乙的溶解度 ;
(2)在温度不变的情况下,把乙的不饱和容液变为饱和溶液的方法是 ;
(3)甲中含有少量的乙,若提纯甲应采用的结晶方法是 。
16.结合化学知识回答下列问题。
(1)试举一个能说明分子之间有间隔的例子: ;
(2)CO2与CO的化学性质有很大不同的原因是 。
(1)试举一个能说明分子之间有间隔的例子: ;
(2)CO2与CO的化学性质有很大不同的原因是 。
17.用铝丝、洁净的铜丝、稀盐酸、AgNO3溶液,验证Al、Cu Ag的活动性顺序。
(1)把打磨过的铝丝和洁净的铜丝分别浸入稀盐酸中,观察到铝丝表面有气泡产生,铜丝表面无明显现象,由此判断出Al和Cu的活动性强弱顺序为 >(H)> ;发生反应的基本反应类型是 ;铝丝使用前需用砂纸打磨的原因是 ;
(2)为了达到实验目的,除(1)中实验外,还需要进行的实验是 。
(1)把打磨过的铝丝和洁净的铜丝分别浸入稀盐酸中,观察到铝丝表面有气泡产生,铜丝表面无明显现象,由此判断出Al和Cu的活动性强弱顺序为 >(H)> ;发生反应的基本反应类型是 ;铝丝使用前需用砂纸打磨的原因是 ;
(2)为了达到实验目的,除(1)中实验外,还需要进行的实验是 。
18.如图是实验室制取气体的常用装置。

(1)仪器①的名称是 ;
(2)选择恰当的装置,可用来加热高锰酸钾制取氧气,发生反应的化学方程式为 ;用E装置收集氧气时,待集气瓶里的水排完后, ,再小心地把集气瓶移出水槽,正放在桌面上。
(3)实验室制取二氧化碳气体,应选择的发生装置和最佳收集装置是 。

(1)仪器①的名称是 ;
(2)选择恰当的装置,可用来加热高锰酸钾制取氧气,发生反应的化学方程式为 ;用E装置收集氧气时,待集气瓶里的水排完后, ,再小心地把集气瓶移出水槽,正放在桌面上。
(3)实验室制取二氧化碳气体,应选择的发生装置和最佳收集装置是 。
19.某化学兴趣小组的同学们在实验室里探究某些酸、碱、盐之间是否发生复分解反应。
【查阅资料】硫酸钡(BaSO4)白色固体,不溶于水,也不溶于盐酸、硫酸和硝酸。
【实验与探究】
实验三结束后,某同学出于好奇,把实验三试管里的上层清液a倒入另一支洁净的试管中,向清液a中逐滴滴加K2CO3溶液。在滴加过程中,发现先产生气泡,然后又产生白色沉淀。根据上述现象,请你判断原清液a中的溶质是⑤ 。
【拓展与应用】将稀盐酸Ca(OH)2溶液NaCl溶液Na2CO3溶液任意两种溶液相混合,写出能发生反应且有沉淀生成的化学方程式 。
【查阅资料】硫酸钡(BaSO4)白色固体,不溶于水,也不溶于盐酸、硫酸和硝酸。
【实验与探究】
| 内容 | 现象 | 实验解析 | 结论 | |
| 实验一 |  | ① | 化学方程式是:K2CO3+H2SO4═K2SO4+H2O+CO2↑ | 生成物中有气体或有④ 或有沉淀生成时,复分解反应可以发生。 |
| 实验二 | 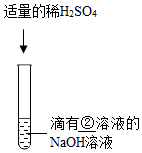 ② | 溶液颜色由红色恰好变为无色 |  ③ | |
| 实验三 | 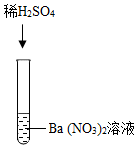 | 产生白色沉淀 | 该反应的实质是:Ba2++SO42-═BaSO4↓ |
实验三结束后,某同学出于好奇,把实验三试管里的上层清液a倒入另一支洁净的试管中,向清液a中逐滴滴加K2CO3溶液。在滴加过程中,发现先产生气泡,然后又产生白色沉淀。根据上述现象,请你判断原清液a中的溶质是⑤ 。
【拓展与应用】将稀盐酸Ca(OH)2溶液NaCl溶液Na2CO3溶液任意两种溶液相混合,写出能发生反应且有沉淀生成的化学方程式 。
20.现有溶质质量分数为20%的NaOH溶液20g,与一定质量的稀盐酸恰好完全反应。
计算:(1)NaOH溶液中溶质的质量为 g
(2)生成NaCl的质量。
计算:(1)NaOH溶液中溶质的质量为 g
(2)生成NaCl的质量。
查看全部题目