下载高清试卷
【2020年湖北省武汉市中考化学试卷】-第1页
试卷格式:2020年湖北省武汉市中考化学试卷.PDF
试卷热词:最新试卷、2020年、湖北试卷、武汉市试卷、化学试卷、九年级试卷、中考试卷、初中试卷
扫码查看解析
试卷题目
1.下列物质中属于单质的是( )
- A. 五氧化二磷
- B. 铜
- C. 稀盐酸
- D. 高锰酸钾
2.下列实验操作正确的是( )
- A.
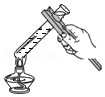 加热液体
加热液体 - B.
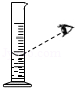 俯视读数
俯视读数 - C.
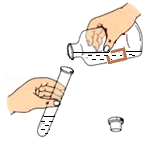 倾倒液体
倾倒液体 - D.
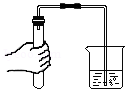 检查气密性
检查气密性
3.下列化学用语正确的是( )
- A. 2个氮原子表示为2N
- B. 氯化钠的化学式为ClNa
- C. 氧气中O为﹣2价
- D. S2﹣的结构示意图为

4.下列说法正确的是( )
- A. 物体受热膨胀是因为分子体积变大
- B. pH<7的溶液能使酚酞变红
- C. 焚烧含氯塑料会造成空气污染
- D. 长期大量施用化肥不会影响环境
5.化学概念在逻辑上存在并列、交叉和包含关系,可用如图表示这三种关系。以下关系界定错误的是( )


- A. 合金和金属材料属于包含关系
- B. 金属元素和非金属元素属于并列关系
- C. 盐和化合物属于包含关系
- D. 物理变化和化学变化属于交叉关系
6.如图涉及的物质及变化均为初中化学常见的纯净物及化学反应,其中乙、丙、丁在通常状况下为三种不同状态的氧化物。图中“﹣”表示两物质之间能发生反应,“→”表示两物质之间能发生一步转化。 下列说法正确的是( )


- A. 甲可以是由四种元素组成的化合物
- B. 若甲经一步反应同时生成乙和丙,则甲不可能是单质或氧化物
- C. 戊可以是碱,能用于治疗胃酸过多
- D. 丁→戊的反应过程中会吸收大量的热
7.有一包固体粉末X可能含有锌、铁、氧化铜中的一种或几种。 为探究其成分,将m g固体粉末加入到一定质量的稀盐酸中,充分反应后剩余n g固体。下列说法正确的是( )
- A. 若固体粉末X含有铁,则m可能小于n
- B. 若充分反应后溶液中含有四种阳离子,则剩余固体一定为纯净物
- C. 若充分反应后溶液中含有三种阳离子,则固体粉末X一定由三种物质组成
- D. 剩余n g固体可能由铁和氧化铜组成
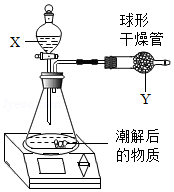
8.小余取8.0g干燥的氢氧化钠固体于敞口的锥形瓶中,观察到氢氧化钠固体发生潮解,一段时间后测得锥形瓶内物质质量为10.0g。为进一步探究上述现象的成因,小余立即用如图装置进行实验:将试剂X逐滴滴入锥形瓶中,直至不再产生气泡为止,测得装置前后质量减少了1.1g。(不考虑滴加液体体积、气体密度变化和结晶水的生成)
下列推断正确的是( )
①试剂X可以是稀硫酸
②固体Y可以是生石灰
③滴加试剂X前锥形瓶内水的质量为0.9g
④若没有球形干燥管,测得氢氧化钠固体从空气中吸收水的质量会偏小
下列推断正确的是( )
①试剂X可以是稀硫酸
②固体Y可以是生石灰
③滴加试剂X前锥形瓶内水的质量为0.9g
④若没有球形干燥管,测得氢氧化钠固体从空气中吸收水的质量会偏小

- A. ①③
- B. ①④
- C. ②③
- D. ②④
9.氧气是一种重要的气体。小颖在试管中加入5mL 5%过氧化氢溶液,再依次进行实验:①插入带有火星的木条;②加入少量二氧化锰;③插入带有火星的木条。
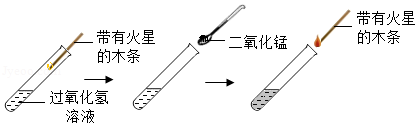
(1)当出现带有火星的木条 的现象时,说明试管中有大量氧气产生。
(2)实验③中产生氧气的化学方程式为 ,该反应属于 (填基本反应类型)。

(1)当出现带有火星的木条 的现象时,说明试管中有大量氧气产生。
(2)实验③中产生氧气的化学方程式为 ,该反应属于 (填基本反应类型)。
10.将30g固体物质X(不含结晶水)投入盛有20g水的烧杯中,搅拌,测得0℃、t1℃、t2℃、t3℃时烧杯中溶液的质量分别如图中A、B、C、D点所示。回答下列问题:
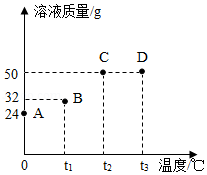
(1)A、B两点对应的溶液中溶质的质量分数较大的是 (填字母编号)。
(2)0℃时,物质X的溶解度是 。
(3)A、B、C、D四点对应的溶液中,一定属于饱和溶液的是 (填字母编号)。
(4)下列说法正确的是 (填序号)。
①t1℃时,若向B点对应的烧杯中再加入30g水,搅拌,所得溶液为不饱和溶液
②若要从D点对应的溶液中得到全部固体X,可采用降温结晶的方法
③t1℃时,将物质X的饱和溶液变为不饱和溶液,溶质的质量可能增大

(1)A、B两点对应的溶液中溶质的质量分数较大的是 (填字母编号)。
(2)0℃时,物质X的溶解度是 。
(3)A、B、C、D四点对应的溶液中,一定属于饱和溶液的是 (填字母编号)。
(4)下列说法正确的是 (填序号)。
①t1℃时,若向B点对应的烧杯中再加入30g水,搅拌,所得溶液为不饱和溶液
②若要从D点对应的溶液中得到全部固体X,可采用降温结晶的方法
③t1℃时,将物质X的饱和溶液变为不饱和溶液,溶质的质量可能增大
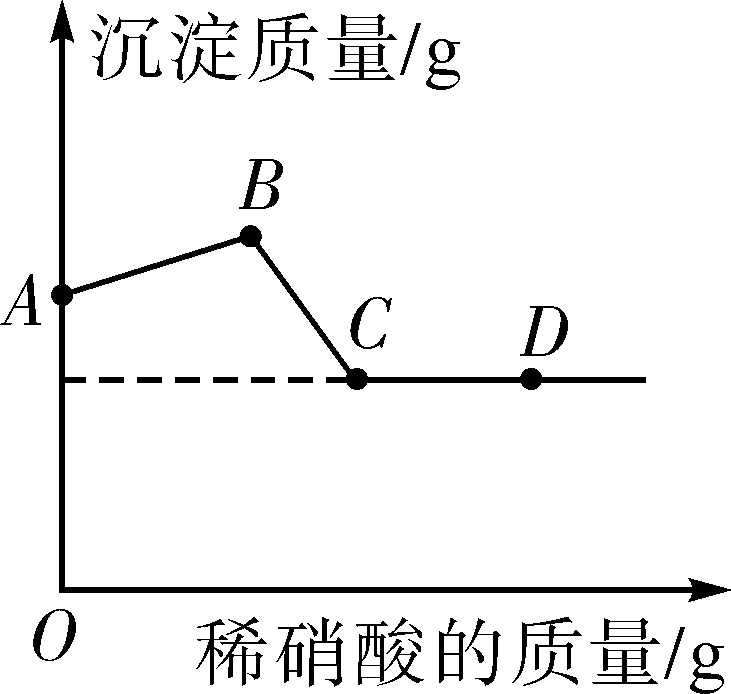
11.如图1所示,小瑾将反应后试管中的物质全部倒入烧杯时,发现烧杯内白色沉淀明显增多。为了探究烧杯内物质的成分,她立即向其中逐滴加入稀硝酸,并不断搅拌,烧杯内沉淀的质量随加入稀硝酸的质量变化如图2所示。
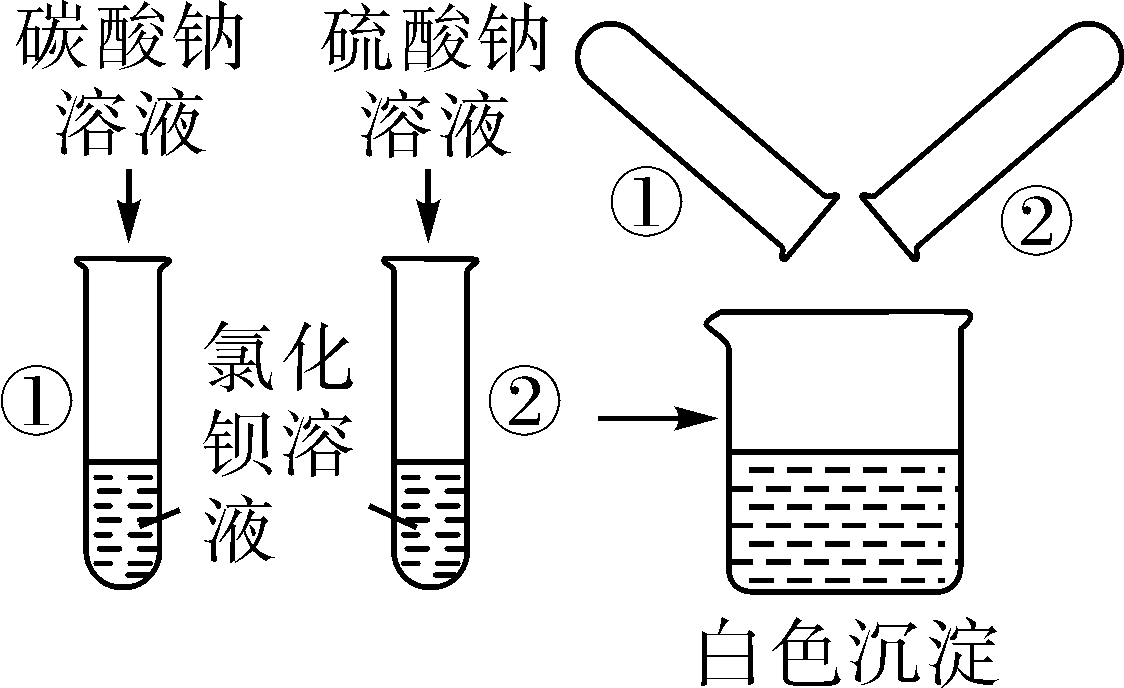
回答下列问题:
(1)图1所示,烧杯内的白色沉淀是 。
(2)BC段发生反应的化学方程式为 。
(3)A点,烧杯内的溶液中一定大量含有的离子为 (写离子符号)。B点,烧杯内的沉淀由 种物质组成。
(4)检验D点溶液中含有氯离子的方法 。


回答下列问题:
(1)图1所示,烧杯内的白色沉淀是 。
(2)BC段发生反应的化学方程式为 。
(3)A点,烧杯内的溶液中一定大量含有的离子为 (写离子符号)。B点,烧杯内的沉淀由 种物质组成。
(4)检验D点溶液中含有氯离子的方法 。
12.实验室有一包久置的生铁粉末(成分为碳、铁和氧化铁)。为测定各组分的质量分数,小怡取两份质量均为m的生铁粉末样品,分别进行如图实验。
Ⅰ.测定碳的含量

已知:过氧化氢溶液能将Fe2+转化为Fe3+。
(1)步骤①的具体实验操作中包括过滤,此操作中玻璃棒的作用是 。
(2)生成滤渣丙的化学方程式为 。
Ⅱ.测定氧化铁的质量分数
如图所示装置气密性良好。在硬质玻璃管中放入样品2。打开止水夹K,在球形干燥管出口处检验氢气纯净后,点燃酒精灯,待充分反应后,熄灭酒精灯,冷却至室温,关闭止水夹K。

(3)打开止水夹K,观察到装置甲中的实验现象是 。
(4)若无装置乙,会导致测得氧化铁的质量分数 (填“偏大”“偏小”或“不变”)。
(5)实验过程中无污染性气体生成,且实验结束,硬质玻璃管中剩余固体为单质铁,丁装置中浓硫酸质量比实验前增重了0.54g。则m= g(结果精确到0.01)。
Ⅰ.测定碳的含量

已知:过氧化氢溶液能将Fe2+转化为Fe3+。
(1)步骤①的具体实验操作中包括过滤,此操作中玻璃棒的作用是 。
(2)生成滤渣丙的化学方程式为 。
Ⅱ.测定氧化铁的质量分数
如图所示装置气密性良好。在硬质玻璃管中放入样品2。打开止水夹K,在球形干燥管出口处检验氢气纯净后,点燃酒精灯,待充分反应后,熄灭酒精灯,冷却至室温,关闭止水夹K。

(3)打开止水夹K,观察到装置甲中的实验现象是 。
(4)若无装置乙,会导致测得氧化铁的质量分数 (填“偏大”“偏小”或“不变”)。
(5)实验过程中无污染性气体生成,且实验结束,硬质玻璃管中剩余固体为单质铁,丁装置中浓硫酸质量比实验前增重了0.54g。则m= g(结果精确到0.01)。
13.乙醇(C2H5OH)俗称酒精,可用作酒精灯、内燃机等的燃料。
(1)燃着的酒精灯用灯帽盖灭,是破坏了 这一燃烧条件。
(2)现有10.0g质量分数为92.0%的酒精的水溶液,在充满足量氧气的密闭容器里充分燃烧后,冷却至室温,求密闭容器内水的质量(结果精确到0.1g)。
(1)燃着的酒精灯用灯帽盖灭,是破坏了 这一燃烧条件。
(2)现有10.0g质量分数为92.0%的酒精的水溶液,在充满足量氧气的密闭容器里充分燃烧后,冷却至室温,求密闭容器内水的质量(结果精确到0.1g)。
查看全部题目