下载高清试卷
【2020-2021学年山东省威海市文登区九年级(上)期末化学试卷(五四学制)】-第1页
试卷格式:2020-2021学年山东省威海市文登区九年级(上)期末化学试卷(五四学制).PDF
试卷热词:最新试卷、2021年、山东试卷、威海市试卷、化学试卷、九年级上学期试卷、期末试卷、初中试卷
扫码查看解析
试卷题目
1.下列过程中没有发生化学变化的是( )
- A. 牛奶发酵过程中某些菌种使牛奶中的部分蛋白质被分解成小分子
- B. 利用膜法从海水中获得淡水
- C. 海水制镁
- D. 用75%酒精杀菌消毒
2.下列关于溶液的说法错误的是( )
- A. 与乳化作用相比,溶解能使物质混合得更均匀
- B. 溶液都是由溶质和溶剂组成的,溶质质量分数和体积分数都可以定量表示溶液的组成
- C. 海水“晒盐”后剩余的苦卤一定是食盐的饱和溶液
- D. 向溶液中加入溶质后溶质质量分数可能会变大,析出晶体后溶质质量分数一定会变小
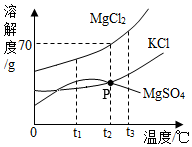
3.如图是MgCl2、KCl和MgSO4的溶解度曲线。下列说法中错误的个数是( )
①一定温度下,三种物质的溶解度不随水的质量改变而改变
②t1℃时三种物质的饱和溶液中,溶质质量分数最大的是MgCl2
③将t3℃时氯化钾和硫酸镁的饱和溶液降温至t2℃时,两溶液溶质质量分数相等
④t2℃时,50g氯化镁的饱和溶液中溶解了35g氯化镁
⑤将t2℃时的三种物质的饱和溶液分别升温至t3℃,会析出晶体的是MgSO4
①一定温度下,三种物质的溶解度不随水的质量改变而改变
②t1℃时三种物质的饱和溶液中,溶质质量分数最大的是MgCl2
③将t3℃时氯化钾和硫酸镁的饱和溶液降温至t2℃时,两溶液溶质质量分数相等
④t2℃时,50g氯化镁的饱和溶液中溶解了35g氯化镁
⑤将t2℃时的三种物质的饱和溶液分别升温至t3℃,会析出晶体的是MgSO4

- A. 1个
- B. 2个
- C. 3个
- D. 4个
4.下列生活中的做法不正确的是( )
- A. 胃酸过多的病人,可服用含氢氧化铝的药物中和过量的胃酸
- B. 重金属盐中毒可喝牛奶、豆浆等食品缓解中毒现象
- C. 吗啡、海洛因、摇头丸等有一定的药用价值,可少量吸食
- D. 变质发霉的食物即使经过高温蒸煮也不能食用
5.山梨酸钾(C6H7COOK)为白色固体,由离子构成,水溶液的pH约为8,是一种常用的食品添加剂,由于它价格偏高,有些不法商家在其中掺入碳酸钾作假,碳酸钾不具备防腐作用。下列有关山梨酸钾和食品添加剂的认识正确的是( )
- A. 山梨酸钾能有效保持食品的新鲜,可以按安全标准量添加
- B. 山梨酸钾中起防腐作用的是钾离子
- C. 山梨酸钾是一种碱
- D. 天然的食品添加剂是对健康无害的,而人工合成的食品添加剂是对人体有害的
6.下列说法科学的是( )
- A. 服用乳酸亚铁糖浆可以治疗骨质疏松
- B. 葡萄糖酸锌口服液、维D钙片、加碘食盐中含人体所需的锌、钙、碘等微量元素
- C. 各种面食中富含淀粉,淀粉在人体内最终变成葡萄糖
- D. 用灼烧闻气味的方法可以检验某食品中是否含有蛋白质
7.我国科学家侯德榜创立“侯氏制碱法”,为纯碱和化肥工业的发展做出了杰出贡献,图1是侯氏制碱法的反应原理,图2是相关物质的溶解度曲线,反应控温30℃,下列说法不正确的是( )


- A. 该过程中除水外,能够循环利用的物质是二氧化碳和NaCl溶液
- B. 30℃时,碳酸氢钠的溶解度小于氯化铵,因此制碱过程中首先析出的是碳酸氢钠
- C. 制得的纯碱中含有少量小苏打可用稀盐酸除去
- D. 侯氏制碱法保留了氨碱法的优点,减少了环境污染,提高了原料利用率
8.某同学设计了探究Zn、Cu、Ag三种金属活动性顺序的实验方案,仅用组内试剂,无法完成的是( )
- A. Zn、Cu、Ag、稀硫酸
- B. Cu、ZnSO4溶液、AgNO3溶液
- C. Zn、Ag、CuSO4溶液
- D. Zn、Cu、稀硫酸、AgNO3溶液
9.下列实验操作能达到实验目的的是( )
| 选项 | 实验目的 | 实验操作 |
| A | 稀释浓硫酸 | 将浓硫酸沿容器壁慢慢注入盛水的量筒中,用玻璃棒搅拌 |
| B | 分离氯化钾和二氧化锰的固体混合物 | 溶解,过滤,洗涤,干燥 |
| C | 除去二氧化碳中的氯化氢 | 通过盛有氢氧化钠溶液的洗气瓶 |
| D | 除去硫酸镁溶液中的硫酸 | 加入过量的氧化镁,过滤 |
- A. A
- B. B
- C. C
- D. D
10.下列图像不能正确反映其对应实验过程中相关量的变化关系的是( )
- A.
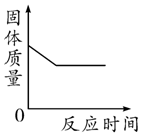 将一氧化碳通过盛有一定量炽热氧化铁的硬质玻璃管
将一氧化碳通过盛有一定量炽热氧化铁的硬质玻璃管 - B.
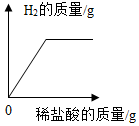 向装有未打磨的铝片的试管中逐渐加入稀盐酸
向装有未打磨的铝片的试管中逐渐加入稀盐酸 - C.
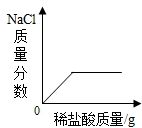 向一定量的氢氧化钠溶液中逐滴加入稀盐酸至过量
向一定量的氢氧化钠溶液中逐滴加入稀盐酸至过量 - D.
 等体积、等浓度的稀盐酸分别与足量铁粉和镁粉反应
等体积、等浓度的稀盐酸分别与足量铁粉和镁粉反应
11.宏观辨识与微观探析。
我们生活在物质的世界,学习化学可以让我们更好的认识和应用物质,下列现象都是由化学变化引起的:①氮肥氯化铵与熟石灰混用会降低肥效;②用铁桶配制波尔多液会降低药效;③点燃酒精灯,酒精燃烧放出大量的热;④将稀盐酸和醋酸滴到紫色牵牛花瓣上,紫色牵牛花瓣都会变红。
(1)宏观物质的微观构成。
在下表中填写物质的化学式、构成物质微粒的符号及物质类别。
(2)宏观变化的微观实质。
宏观变化是构成物质的微粒相互作用的结果,上述①②③在发生化学变化的过程中,发生有效的相互作用而促使变化发生的徽粒分别是① ,② ,③ 。请另写一个与反应①反应物不同,但反应实质相同的化学方程式 。
(3)宏观现象的微观解释。
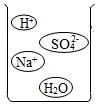
请从微观的角度解释④中产生相同现象的原因 。通过分析组成和结构,也可以预测物质的某些性质。根据如图硫酸氢钠溶液的微观图示,分析推测NaHSO4的性质,其中合理的是 。
A. 其水溶液能使紫色石蕊试液变红
B. 其水溶液能与金属锌反应生成氢气
C. 其水溶液能与硝酸钡溶液反应生成硫酸钡沉淀
D. 其水溶液能与金属镁发生置换反应得到金属钠
我们生活在物质的世界,学习化学可以让我们更好的认识和应用物质,下列现象都是由化学变化引起的:①氮肥氯化铵与熟石灰混用会降低肥效;②用铁桶配制波尔多液会降低药效;③点燃酒精灯,酒精燃烧放出大量的热;④将稀盐酸和醋酸滴到紫色牵牛花瓣上,紫色牵牛花瓣都会变红。
(1)宏观物质的微观构成。
在下表中填写物质的化学式、构成物质微粒的符号及物质类别。
| 物质名称 | 化学式 | 构成物质的微粒 | 物质类别 |
| 氯化铵 | |||
| 铁 | |||
| 酒精 |
(2)宏观变化的微观实质。
宏观变化是构成物质的微粒相互作用的结果,上述①②③在发生化学变化的过程中,发生有效的相互作用而促使变化发生的徽粒分别是① ,② ,③ 。请另写一个与反应①反应物不同,但反应实质相同的化学方程式 。
(3)宏观现象的微观解释。
请从微观的角度解释④中产生相同现象的原因 。通过分析组成和结构,也可以预测物质的某些性质。根据如图硫酸氢钠溶液的微观图示,分析推测NaHSO4的性质,其中合理的是 。
A. 其水溶液能使紫色石蕊试液变红
B. 其水溶液能与金属锌反应生成氢气
C. 其水溶液能与硝酸钡溶液反应生成硫酸钡沉淀
D. 其水溶液能与金属镁发生置换反应得到金属钠

12.手机中的化学。
手机已经成为日常生活中必不可少的通讯工具,如图是某品牌的一款手机,请回答下列问题。
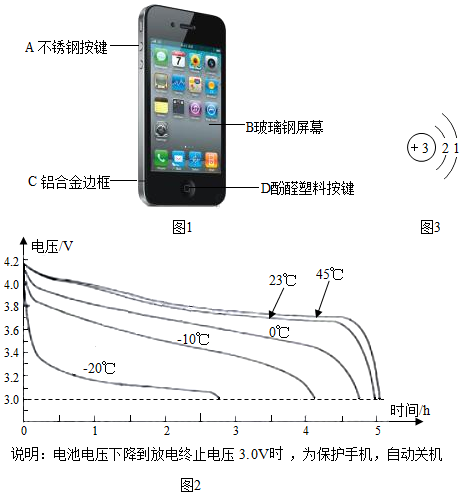
(1)图1所用材料属于合金的是 (填字母序号)。玻璃钢具有诸多优点,可以作为替代金属和塑料的理想材料。请写出玻璃钢作为替代材料的优点(写两条即可): 。
(2)手机所用电池具有质量轻,充电时间短,放电时间长等优点,某种锂电池的工作原理是FePO4+Li
LiFePO4,放电时的能量转化为 → 。
(3)如图2是某款锂电池手机在不同温度下的电压随时间变化的图像,请结合图像分析手机电池冬天不耐用的原因是 。
(4)最早采用电解熔融氯化锂的方法制取锂,图3是锂原子结构示意图,该反应的化学方程式为 。
(5)我国每年报废的手机超过1亿部。废旧手机的电路板中含有多种金属,随意丢弃会造成资源浪费并污染土壤和水体。某手机电路板中含有Sn、Fe、Cu、Au、Ag等金属,如图4是某工厂回收其中部分金属的流程图。(其中Sn、Au在化合物中的化合价分别为+2价、+3价)
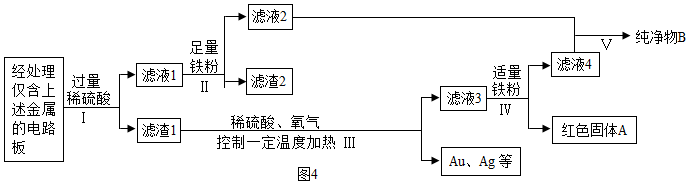
①过程Ⅰ、Ⅱ、Ⅳ均涉及的操作是 。完成此操作需要的仪器有 。操作Ⅴ的名称是 。
②写出过程Ⅱ中反应的化学方程式 。
③写出过程Ⅲ中反应的化学方程式 。
④滤液4中的溶质是 。
⑤若步骤Ⅳ实验过程中加入铁粉前后溶液中主要离子变化示意图如图5所示。

图中“ ”所代表粒子的符号为 。
”所代表粒子的符号为 。
(6)智能手机屏幕解锁图形如图6所示,若以氧化铜为起点,相邻之间可以反应就可以连接,当连接了五个点才可以开锁。请写出解锁路径:CuO﹣ ﹣ ﹣ ﹣ 。
手机已经成为日常生活中必不可少的通讯工具,如图是某品牌的一款手机,请回答下列问题。

(1)图1所用材料属于合金的是 (填字母序号)。玻璃钢具有诸多优点,可以作为替代金属和塑料的理想材料。请写出玻璃钢作为替代材料的优点(写两条即可): 。
(2)手机所用电池具有质量轻,充电时间短,放电时间长等优点,某种锂电池的工作原理是FePO4+Li
放电 |
充电 |
(3)如图2是某款锂电池手机在不同温度下的电压随时间变化的图像,请结合图像分析手机电池冬天不耐用的原因是 。
(4)最早采用电解熔融氯化锂的方法制取锂,图3是锂原子结构示意图,该反应的化学方程式为 。
(5)我国每年报废的手机超过1亿部。废旧手机的电路板中含有多种金属,随意丢弃会造成资源浪费并污染土壤和水体。某手机电路板中含有Sn、Fe、Cu、Au、Ag等金属,如图4是某工厂回收其中部分金属的流程图。(其中Sn、Au在化合物中的化合价分别为+2价、+3价)

①过程Ⅰ、Ⅱ、Ⅳ均涉及的操作是 。完成此操作需要的仪器有 。操作Ⅴ的名称是 。
②写出过程Ⅱ中反应的化学方程式 。
③写出过程Ⅲ中反应的化学方程式 。
④滤液4中的溶质是 。
⑤若步骤Ⅳ实验过程中加入铁粉前后溶液中主要离子变化示意图如图5所示。

图中“
 ”所代表粒子的符号为 。
”所代表粒子的符号为 。(6)智能手机屏幕解锁图形如图6所示,若以氧化铜为起点,相邻之间可以反应就可以连接,当连接了五个点才可以开锁。请写出解锁路径:CuO﹣ ﹣ ﹣ ﹣ 。
13.金属的锈蚀与防护。
小林学习金属的相关知识后,关注到生活中有以下现象:切过咸菜的菜刀,不及时清洗,很容易就锈蚀了,小林同学为探究该现象,做了如图1所示实验:

实验现象:①②7天后铁钉表面无变化,③2天后铁钉表面出现红色,④1天后铁钉表面出现红色。
(1)该方案中采用了对照实验的方法,能获得铁生锈与氧气、与水有关的对照实验分别是(填实验编号) 和 。通过上述实验现象的分析可知,切过咸菜的菜刀,不及时清洗,很容易就锈蚀了的原因是 。
(2)防止切过咸菜的菜刀生锈的措施 。
(3)小林同学发现家中有一瓶除锈剂,可用来除去菜刀表面的锈,回想起化学课上学过的稀盐酸和稀硫酸均可用于金属表面除锈,为探究除锈剂的成分,小林在老师的指导下开展了实验(如图2):
①图2中可以用来检验该除锈剂中是否含有酸的试剂有 (填数字编号,下同)。
②图2中的 可用来确定该除锈剂的成分是稀盐酸还是稀硫酸。从微观角度解释该反应可用于区分稀盐酸和稀硫酸的原因 。
③经探究确定该除锈剂的主要成分是稀硫酸,则用除锈剂除铁锈过程中发生化学反应的方程式为 (不考虑其它成分发生的化学反应)。
④实验室欲用98%(密度为1.84g/mL)的浓硫酸配制100mL 9.8%密度为1.1g/mL)的稀硫酸用于除锈,则需量取水的体积为 mL。
小林学习金属的相关知识后,关注到生活中有以下现象:切过咸菜的菜刀,不及时清洗,很容易就锈蚀了,小林同学为探究该现象,做了如图1所示实验:

实验现象:①②7天后铁钉表面无变化,③2天后铁钉表面出现红色,④1天后铁钉表面出现红色。
(1)该方案中采用了对照实验的方法,能获得铁生锈与氧气、与水有关的对照实验分别是(填实验编号) 和 。通过上述实验现象的分析可知,切过咸菜的菜刀,不及时清洗,很容易就锈蚀了的原因是 。
(2)防止切过咸菜的菜刀生锈的措施 。
(3)小林同学发现家中有一瓶除锈剂,可用来除去菜刀表面的锈,回想起化学课上学过的稀盐酸和稀硫酸均可用于金属表面除锈,为探究除锈剂的成分,小林在老师的指导下开展了实验(如图2):
①图2中可以用来检验该除锈剂中是否含有酸的试剂有 (填数字编号,下同)。
②图2中的 可用来确定该除锈剂的成分是稀盐酸还是稀硫酸。从微观角度解释该反应可用于区分稀盐酸和稀硫酸的原因 。
③经探究确定该除锈剂的主要成分是稀硫酸,则用除锈剂除铁锈过程中发生化学反应的方程式为 (不考虑其它成分发生的化学反应)。
④实验室欲用98%(密度为1.84g/mL)的浓硫酸配制100mL 9.8%密度为1.1g/mL)的稀硫酸用于除锈,则需量取水的体积为 mL。
14.探究石灰石分解。
《天工开物》中有“煤饼烧石成灰”的记载,实验课上,同学们对“烧石(石灰石)成灰”展开深入探究。
(1)为证明石灰石已分解,甲同学按如图所示进行实验,观察到烧杯内壁澄清石灰水变浑浊,从而得出石灰石已分解的结论,你认为甲同学的方案是否合理?为什么? 。
(2)为探究锻烧后“灰”的主要成分,小组同学设计并进行实验,请将如表填写完整[石灰石中的杂质不溶于水,也不参与反应]
依据上述实验证据,小组同学推理得出:锻烧后的“灰”中含有生石灰和碳酸钙。检验物质应用了物质的性质,上述你设计的方案中应用了相关物质的哪些性质? 。
(3)物质的性质决定了物质的用途。战国时《周礼》中记载沿海古人“煤饼烧蛎房成灰”(“蛎房”即牡蛎壳,主要成分是碳酸钙),并把这种灰称为“蜃”。“蜃”与草木灰(主要成分为碳酸钾)、水混合后所得的溶液可用来洗涤帛丝。写出上述反应过程中发生化学变化的方程式 。其化学反应的基本类型分别是 。

《天工开物》中有“煤饼烧石成灰”的记载,实验课上,同学们对“烧石(石灰石)成灰”展开深入探究。
(1)为证明石灰石已分解,甲同学按如图所示进行实验,观察到烧杯内壁澄清石灰水变浑浊,从而得出石灰石已分解的结论,你认为甲同学的方案是否合理?为什么? 。
(2)为探究锻烧后“灰”的主要成分,小组同学设计并进行实验,请将如表填写完整[石灰石中的杂质不溶于水,也不参与反应]
| 实验方案 | 现象 |
依据上述实验证据,小组同学推理得出:锻烧后的“灰”中含有生石灰和碳酸钙。检验物质应用了物质的性质,上述你设计的方案中应用了相关物质的哪些性质? 。
(3)物质的性质决定了物质的用途。战国时《周礼》中记载沿海古人“煤饼烧蛎房成灰”(“蛎房”即牡蛎壳,主要成分是碳酸钙),并把这种灰称为“蜃”。“蜃”与草木灰(主要成分为碳酸钾)、水混合后所得的溶液可用来洗涤帛丝。写出上述反应过程中发生化学变化的方程式 。其化学反应的基本类型分别是 。

15.测定氢氧化钠的质量分数。
某学习小组对课本中“食盐常用于制氯气、烧碱”的内容产生兴趣。小组同学用自制的实验装置(主体部分如图所示)进行电解饱和食盐水制取氢氧化钠的实验(忽略其他可能发生的反应对实验的影响)。实验过程中发生反应的化学方程式是2NaCl+2H2O
2NaOH+H2↑+Cl2↑。一段时间后,关闭电源,从K处导出40g待测液,向其中逐滴加入质量分数为4.9%的稀硫酸至pH等于7,测得反应后溶液的总质量为140g,试计算待测液中氢氧化钠的质量分数。
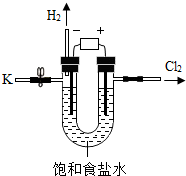
某学习小组对课本中“食盐常用于制氯气、烧碱”的内容产生兴趣。小组同学用自制的实验装置(主体部分如图所示)进行电解饱和食盐水制取氢氧化钠的实验(忽略其他可能发生的反应对实验的影响)。实验过程中发生反应的化学方程式是2NaCl+2H2O
| 通电 |

查看全部题目
相关试卷推荐
更多热门试卷
如何查看答案以及解析
扫描右侧二维码查看试卷答案解析以及视频讲解