下载高清试卷
【2020-2021学年天津市河西区九年级(上)期末化学试卷】-第1页
试卷格式:2020-2021学年天津市河西区九年级(上)期末化学试卷.PDF
试卷热词:最新试卷、2021年、天津试卷、河西区试卷、化学试卷、九年级上学期试卷、期末试卷、初中试卷

扫码查看解析
试卷题目
1.下列元素中,属于金属元素的是( )
- A. 硅
- B. 氯
- C. 磷
- D. 钠
2.下列物质中,富含糖类的是( )
- A. 鸡蛋
- B. 面包
- C. 牛肉
- D. 菠菜
3.马铃薯是非常好的高钾低钠食品,很适合肥胖者食用。这里的“钠、钾”是指( )
- A. 元素
- B. 分子
- C. 原子
- D. 离子
4.下列安全标志中,表示“禁止燃放鞭炮”的是( )
- A.

- B.

- C.

- D.

5.从环境保护的角度考虑,下列燃料中最理想的是( )
- A. 氢气
- B. 一氧化碳
- C. 酒精
- D. 乙醇汽油
6.下列物质的用途中,利用其化学性质的是( )
- A. 铜用于制作导线
- B. 干冰用作制冷剂
- C. 赤铁矿用于炼铁
- D. 金刚石用于裁玻璃
7.金刚石、石墨和C60的化学性质相似,物理性质却有大差异,其主要原因是( )
- A. 构成它们的原子大小不同
- B. 构成它们的原子状态不同
- C. 构成它们的原子数目不同
- D. 构成它们的原子排列方式不同
8.鉴别下列各组物质的试剂或方法(括号内),不正确的是( )
- A. 硬水和软水(食盐水)
- B. 氧气和氮气(燃着的木条)
- C. 空气和二氧化碳(澄清石灰水)
- D. 水和过氧化氢溶液(二氧化锰粉末)
9.用灯帽盖灭酒精灯的原理是( )
- A. 隔离可燃物
- B. 隔绝空气
- C. 降低酒精的着火点
- D. 降低温度至酒精的着火点以下
10.下列实验操作“先”、“后”顺序,错误的是
( )
( )
- A. 点燃可燃性气体时,先验纯,后点燃
- B. 给试管中固体加热时,先均匀加热试管,后固定加热
- C. 制备气体时,先向装置中加药品,后检查装置气密性
- D. CO还原CuO的实验结束时,先熄灭酒精灯,后停止通CO
11.(多选)下列实验方案中,能达到目的的是( )
- A. 鉴别:用扇闻的方法鉴别二氧化碳和一氧化碳
- B. 提纯:用冷却热饱和溶液的方法提纯含少量氯化钠的硝酸钾
- C. 检验:用加入稀盐酸的方法证明碳酸钠粉末中混有碳酸钙
- D. 除杂:用在空气中灼烧的方法除去氧化铜中的炭粉
12.在一定量的硝酸银和硝酸铜溶液中加入锌粉,充分反应后过滤,得到滤液和滤渣,下列分析正确的是( )
- A. 如果滤液显蓝色,则滤渣一定没有Cu
- B. 如果滤渣只含一种金属,滤液中的溶质可能含有三种
- C. 在滤渣中加入稀盐酸有气泡产生,滤液中的溶质可能含有两种
- D. 在滤渣中加入稀盐酸没有气泡产生,则滤渣一定含有Ag和Cu
13.(多选)如图所示,a、b、c分别是初中化学中常见的固体、气体和液体,气球套在试管口且保证密封性能良好。下列说法不正确的是( )
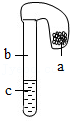

- A. 若b为二氧化碳,c为水,将a倒入试管中,气球会变瘪,则a可能是氢氧化钙
- B. 若b为空气,a为二氧化锰,将a倒入试管中,气球会变鼓,则c可能是过氧化氢溶液
- C. 若b为空气,c为水,将a倒入试管中,气球会变鼓,则a可能是硝酸铵
- D. 若b为空气,c为稀硫酸,将a倒入试管中,气球会变鼓,a可能是铜粉
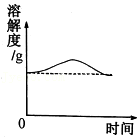
14.(多选)某温度时,向一定量的饱和氢氧化钙溶液中加入少量生石灰,再恢复到原温度,下列各相关的变化图象正确的是( )
- A.

- B.

- C.
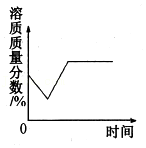
- D.
15.实验室有碳酸钙和碳酸钡的固体混合物50g,加入300g稀盐酸恰好反应,将反应后的溶液蒸干得到54.4g固体。则原混合物中金属元素的质量分数为( )
(已知BaCO3+2HCl═BaCl2+H2O+CO2↑)
(已知BaCO3+2HCl═BaCl2+H2O+CO2↑)
- A. 40%
- B. 48%
- C. 52%
- D. 72%
16.化学就在我们身边。
(1)现有A.汞 B.液氢 C.石墨 D.一氧化碳 E.干冰,请选择适当的物质填空(填序号)。
①属于高能燃料的是 ;
②用于制铅笔芯的是 ;
③常温下呈液态的金属是 ;
④用于食品冷藏保鲜的是 ;
⑤吸烟有害健康,烟气中的一种有毒气体是 。
(2)用化学用语回答下列问题。
①磁铁矿的主要成分是 ;
②海水中含量最高的金属阳离子是 ;
③人体中缺乏 会引起食欲不振,生长迟缓。
(1)现有A.汞 B.液氢 C.石墨 D.一氧化碳 E.干冰,请选择适当的物质填空(填序号)。
①属于高能燃料的是 ;
②用于制铅笔芯的是 ;
③常温下呈液态的金属是 ;
④用于食品冷藏保鲜的是 ;
⑤吸烟有害健康,烟气中的一种有毒气体是 。
(2)用化学用语回答下列问题。
①磁铁矿的主要成分是 ;
②海水中含量最高的金属阳离子是 ;
③人体中缺乏 会引起食欲不振,生长迟缓。
17.取四朵用石蕊溶液染成紫色的干燥纸花,完成图示实验并回答下列问题。
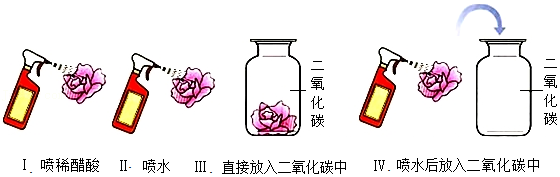
(1)对比实验Ⅰ和Ⅱ,说明水不能使石蕊变红,而 ;
(2)实验Ⅲ中紫色小花 (“变红色”或“不变色”);
(3)完成Ⅰ~Ⅳ实验后,得到的结论是 ;
(4)实验后,将Ⅳ中的小花取出烘干,发生反应的化学方程式为 。

(1)对比实验Ⅰ和Ⅱ,说明水不能使石蕊变红,而 ;
(2)实验Ⅲ中紫色小花 (“变红色”或“不变色”);
(3)完成Ⅰ~Ⅳ实验后,得到的结论是 ;
(4)实验后,将Ⅳ中的小花取出烘干,发生反应的化学方程式为 。
18.能源利用和环境保护是人类共同关注的问题。
(1)化石燃料包括煤、 和天然气等。天然气在空气中充分燃烧的化学方程式为 。
(2)燃煤会影响环境,下列环境问题与燃煤有直接关系的是 (填序号)。
A.酸雨
B.温室效应
C.可吸入颗粒物增加
(3)解决环境问题需要科技进步,如CO2含量不断升高,使全球气候问题日趋严重,人类不仅要努力减少CO2的排放,更重要的是将CO2转化为有用物质。将CO2转化为化工原料乙烯(C2H4),其反应的微观过程如图所示,请写出上述反应的化学方程式 。
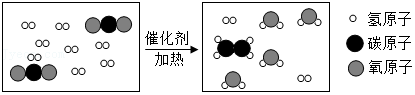
(1)化石燃料包括煤、 和天然气等。天然气在空气中充分燃烧的化学方程式为 。
(2)燃煤会影响环境,下列环境问题与燃煤有直接关系的是 (填序号)。
A.酸雨
B.温室效应
C.可吸入颗粒物增加
(3)解决环境问题需要科技进步,如CO2含量不断升高,使全球气候问题日趋严重,人类不仅要努力减少CO2的排放,更重要的是将CO2转化为有用物质。将CO2转化为化工原料乙烯(C2H4),其反应的微观过程如图所示,请写出上述反应的化学方程式 。

19.写出下列反应的化学方程式。
(1)用木炭粉末还原足量的氧化铜: ;
(2)将铜片放入硝酸银溶液中: ;
(3)用澄清的石灰水检验二氧化碳: 。
(1)用木炭粉末还原足量的氧化铜: ;
(2)将铜片放入硝酸银溶液中: ;
(3)用澄清的石灰水检验二氧化碳: 。
20.溶液与人类生产、生活密切相关。请回答下列问题:
(1)将少量生石灰加入足量的水中,形成的溶液称为 ,溶质为 (填化学式)。
(2)衣服上沾染的油污,可用汽油洗去,是因为汽油能 (填“溶解”或“乳化”)油污。
(3)甲、乙、丙三种固体物质(不含结晶水,且不与水反应)的溶解度曲线如图所示。
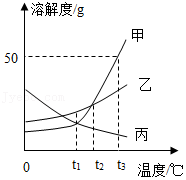
①t1℃时,甲、丙两种物质的溶解度 (填“相等”或“不相等”);
②将丙的饱和溶液变为不饱和溶液,可采用 (填“降低”或“升高”)温度的方法;
③t3℃时,将甲、乙、丙三种物质的饱和溶液分别降温到t1℃,所得溶液中溶质的质量分数大小关系是 (填序号);
A、甲=丙>乙
B、甲=丙<乙
C、甲>乙>丙
D、乙>甲>丙
④t3℃时,将甲的饱和溶液mg加水稀释到2mg,则稀释后溶液中溶质的质量分数为 (计算结果精确到0.1%)。
(1)将少量生石灰加入足量的水中,形成的溶液称为 ,溶质为 (填化学式)。
(2)衣服上沾染的油污,可用汽油洗去,是因为汽油能 (填“溶解”或“乳化”)油污。
(3)甲、乙、丙三种固体物质(不含结晶水,且不与水反应)的溶解度曲线如图所示。

①t1℃时,甲、丙两种物质的溶解度 (填“相等”或“不相等”);
②将丙的饱和溶液变为不饱和溶液,可采用 (填“降低”或“升高”)温度的方法;
③t3℃时,将甲、乙、丙三种物质的饱和溶液分别降温到t1℃,所得溶液中溶质的质量分数大小关系是 (填序号);
A、甲=丙>乙
B、甲=丙<乙
C、甲>乙>丙
D、乙>甲>丙
④t3℃时,将甲的饱和溶液mg加水稀释到2mg,则稀释后溶液中溶质的质量分数为 (计算结果精确到0.1%)。
21.A、B、C、D是初中化学常见的物质,常温下A、B均为无色气体且是组成元素相同的氧化物,C、D均为黑色粉末且D为单质,物质间的转化关系如图所示(部分反应物、生成物及反应条件已略去)。请回答下列问题:
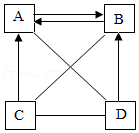
(1)写出体现D的化学性质的用途(填一种): 。
(2)写出相关反应的化学方程式:
①A+D: ;
②B+C: ,此反应类型 (填“是”或“不是”)置换反应。

(1)写出体现D的化学性质的用途(填一种): 。
(2)写出相关反应的化学方程式:
①A+D: ;
②B+C: ,此反应类型 (填“是”或“不是”)置换反应。
22.实验室配制50g溶质质量分数为6%的氯化钠溶液。
(1)需称量氯化钠的质量是 g。称量时,向托盘天平加入一定质量的氯化钠后,发现指针偏右,此时应继续进行的操作是 。
A. 增加适量氯化钠固体
B. 减少适量氯化钠固体
C. 调节平衡螺母
(2)溶解时用到的玻璃仪器有烧杯、 。
(1)需称量氯化钠的质量是 g。称量时,向托盘天平加入一定质量的氯化钠后,发现指针偏右,此时应继续进行的操作是 。
A. 增加适量氯化钠固体
B. 减少适量氯化钠固体
C. 调节平衡螺母
(2)溶解时用到的玻璃仪器有烧杯、 。
23.如图为实验室常用的实验装置,请回答下列问题。
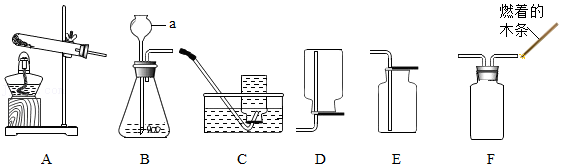
(1)仪器a的名称是 。
(2)实验室用装置A制取氧气,反应的化学方程式为 。
(3)实验室制备二氧化碳应选用的发生装置是 (填序号),该反应的化学方程式为 。若用装置F采用排空气法收集二氧化碳并验满,请将装置F补画完整。

(1)仪器a的名称是 。
(2)实验室用装置A制取氧气,反应的化学方程式为 。
(3)实验室制备二氧化碳应选用的发生装置是 (填序号),该反应的化学方程式为 。若用装置F采用排空气法收集二氧化碳并验满,请将装置F补画完整。
24.金属是人类生活中常用的材料。请回答:
(1)天津地铁4号线预计2021年建成通车。
①地铁列车车体大量使用的铝合金属于 (填“单质“或“混合物”)。
②地铁建造过程中需要使用大量的生铁和钢,两者的主要区别是 。
(2)铁制品锈蚀的过程,实际上是铁跟空气中的 、 等发生化学反应的过程。
(3)为探究锌、铁、铜三种金属的活动性,及其与氢元素的位置关系,下列不需要进行的实验是 (填标号)。
A.将铁片放入稀硫酸中
B.将铁片放入硫酸锌溶液中
C.将铜片放入稀硫酸中
D.将铁片放入硫酸铜溶液中
(4)将光亮的铜片置于潮湿空气中一段时间后,表面出现绿色铜锈[主要成分是碱式碳酸铜Cu2(OH)2CO3]。以铜锈为原料设计并完成图示实验(杂质不与稀硫酸反应,且不含铜元素)。
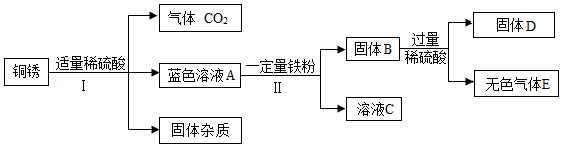
①无色气体E的化学式是 ;
②Ⅱ过程的化学方程式是 ;
③若该铜锈样品的质量是20g,固体D的质量是6.4g,则铜锈中含Cu2(OH)2CO3的质量分数是 。
(1)天津地铁4号线预计2021年建成通车。
①地铁列车车体大量使用的铝合金属于 (填“单质“或“混合物”)。
②地铁建造过程中需要使用大量的生铁和钢,两者的主要区别是 。
(2)铁制品锈蚀的过程,实际上是铁跟空气中的 、 等发生化学反应的过程。
(3)为探究锌、铁、铜三种金属的活动性,及其与氢元素的位置关系,下列不需要进行的实验是 (填标号)。
A.将铁片放入稀硫酸中
B.将铁片放入硫酸锌溶液中
C.将铜片放入稀硫酸中
D.将铁片放入硫酸铜溶液中
(4)将光亮的铜片置于潮湿空气中一段时间后,表面出现绿色铜锈[主要成分是碱式碳酸铜Cu2(OH)2CO3]。以铜锈为原料设计并完成图示实验(杂质不与稀硫酸反应,且不含铜元素)。

①无色气体E的化学式是 ;
②Ⅱ过程的化学方程式是 ;
③若该铜锈样品的质量是20g,固体D的质量是6.4g,则铜锈中含Cu2(OH)2CO3的质量分数是 。
25.现有1000t含Fe2O380%赤铁矿石(杂质中不含铁元素),试计算:
(1)该赤铁矿石含Fe2O3的质量是 t;
(2)该赤铁矿石含铁元素的质量是 t;
(3)理论上可以炼出含铁96%的生铁的质量是 t(计算结果精确至0.1t)。
(1)该赤铁矿石含Fe2O3的质量是 t;
(2)该赤铁矿石含铁元素的质量是 t;
(3)理论上可以炼出含铁96%的生铁的质量是 t(计算结果精确至0.1t)。
26.为了测定某含杂质7%的黄铜(主要含铜锌)样品中铜的质量,取100g该样品(杂质不参加反应也不溶于水),加入盛有100g 14.6%稀盐酸的烧杯中,恰好完全反应,气体全部逸出,过滤,再向滤液中加入87.4g水。
(1)该黄铜样品中铜的质量;
(2)最终所得溶液中溶质的质量分数。
(1)该黄铜样品中铜的质量;
(2)最终所得溶液中溶质的质量分数。
查看全部题目
相关试卷推荐
更多热门试卷
如何查看答案以及解析
扫描右侧二维码查看试卷答案解析以及视频讲解