下载高清试卷
【2021-2022学年上海市长宁区九年级(上)期末化学试卷(一模)】-第1页
试卷格式:2021-2022学年上海市长宁区九年级(上)期末化学试卷(一模).PDF
试卷热词:最新试卷、2022年、上海试卷、长宁区试卷、化学试卷、九年级上学期试卷、期末试卷、初中试卷

扫码查看解析
试卷题目
1.不能改善空气质量的措施是( )
- A. 推广清洁能源
- B. 汽车尾气净化
- C. 控制工地扬尘
- D. 使用空气香薰
2.氢元素符号书写正确的是( )
- A. N
- B. Ne
- C. H
- D. He
3.空气中含量最多的成分是( )
- A. 氧气
- B. 氮气
- C. 氖气
- D. 二氧化碳
4.SO2中硫元素的化合价是( )
- A. +1
- B. +2
- C. +3
- D. +4
5.属于碳的化学性质的是( )
- A. 还原性
- B. 导电性
- C. 导热性
- D. 吸附性
6.自来水生产中,能起到杀菌消毒作用的试剂是( )
- A. 活性炭
- B. 氯气
- C. 砂石
- D. 明矾
7.Na2CO3中原子团的名称是( )
- A. 三氧化碳
- B. 碳酸
- C. 碳酸根
- D. 碳氧根
8.属于分解反应的是( )
- A. 煅烧大理石
- B. 硫的燃烧
- C. 向生石灰中滴加水
- D. 加热木炭与氧化铜的混合物
9.一定能增大二氧化碳在水中溶解度的操作是( )
- A. 边升温边加压
- B. 边降温边加压
- C. 边升温边减压
- D. 边降温边减压
10.室温下,将pH为12的澄清石灰水敞口放置一段时间后,溶液的pH变化可能是( )
- A. 变小为10
- B. 变小为2
- C. 基本不变
- D. 变大为13
11.为了使酒精充分燃烧,做法错误的是( )
- A. 用纯氧替代空气
- B. 使用固体酒精
- C. 将酒精加热为酒精蒸气
- D. 将酒精喷成雾状
12.由一种分子构成的物质不可能是( )
- A. 单质
- B. 化合物
- C. 混合物
- D. 氧化物
13.关于实验室制取氧气的操作,描述正确的是( )
- A. 分别取等量的氯酸钾和二氧化锰,依次加入到试管底部并混合均匀
- B. 由上至下,从右向左组装仪器
- C. 集气瓶装满水,倒放在水槽中,并将导管伸入集气瓶中
- D. 反应停止后,先将导管从水槽中取出,再熄灭酒精灯
14.关于相对原子质量说法正确的是( )
- A. 相对原子质量的单位是kg
- B. 相对原子质量是一个比值,单位是g
- C. 某原子的相对原子质量在数值上是该原子的实际质量的12倍
- D. 相对原子质量越大,原子的实际质量也越大
15.对金刚石和石墨描述正确的是( )
- A. 碳元素都以游离态存在
- B. 碳元素都以化合态存在
- C. 化学性质相同是由于碳原子排列结构相似
- D. 物理性质不同是由于碳原子排列结构不同
16.如图是电解水时相关量的变化关系,纵坐标中“y”表示的物理量(单位)可能是( )
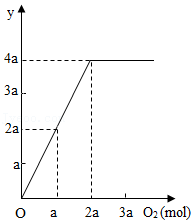

- A. 消耗掉水的物质的量(mol)
- B. 消耗掉水的体积(mL)
- C. 生成氢气的物质的量(mol)
- D. 常温常压下,生成氢气的体积(L)
17.实验室二氧化锰中可能含有炭粉,若直接与大量氯酸钾加热,炭粉在大量氧气中燃烧,引起爆炸,上述反应的化学方程式可能是( )
- A. 8KClO3+MnO2+12C8KCl+12CO2↑+MnO2
△ - B. 8KClO3+2C8KCl+2CO↑+11O2↑
△ - C. 8KClO3+C8KCl+CO2↑+11O2↑
△ - D. 8KClO3+15C8KCl+9CO↑+6O2↑
△
18.我国科学家首次在实验室实现了二氧化碳到淀粉的从头合成。
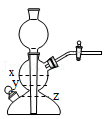
(1)实验室常用块状大理石与稀盐酸制备二氧化碳,该反应的化学方程式是 。选用如图装置作为发生装置,待气体收集满后关闭活塞,装置内液面将由x降至 处(选填“y”或“z”),此时装置内气体压强 外界大气压(选填“大于”、“等于”或“小于”)。
(2)该合成中的第一步是先将二氧化碳转换成甲醇(化学式为CH4O),这属于 (选填“物理”或“化学”)变化,甲醇是由 种元素组成,摩尔质量为 ,1mol甲醇中约含有 个碳原子。
(3)该合成的最后一步是将碳水化合物合成为淀粉,该人工合成淀粉中一定含有氢元素、氧元素和 元素。

(1)实验室常用块状大理石与稀盐酸制备二氧化碳,该反应的化学方程式是 。选用如图装置作为发生装置,待气体收集满后关闭活塞,装置内液面将由x降至 处(选填“y”或“z”),此时装置内气体压强 外界大气压(选填“大于”、“等于”或“小于”)。
(2)该合成中的第一步是先将二氧化碳转换成甲醇(化学式为CH4O),这属于 (选填“物理”或“化学”)变化,甲醇是由 种元素组成,摩尔质量为 ,1mol甲醇中约含有 个碳原子。
(3)该合成的最后一步是将碳水化合物合成为淀粉,该人工合成淀粉中一定含有氢元素、氧元素和 元素。
19.卓筒井手工制盐的工艺流程包括下面五个步骤。
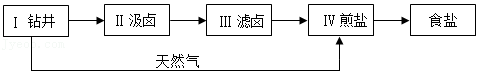
(1)“Ⅱ汲卤”获得卤水为悬浊液,溶液部分中氯化钠的浓度为7%,下表是氯化钠在不同温度时的溶解度。
根据表中数据可得出:20℃时,氯化钠溶解度为 ,该卤水的溶液部分是氯化钠的 (选填“饱和”或“不饱和”)溶液。
(2)“Ⅲ滤卤”与实验操作过滤的原理一样其目的是为了分离溶液和 。
(3)“Ⅳ煎盐”用井中产生的天然气作为燃料,加热卤水,除去其中的溶剂,CH4燃烧的化学方程式是 ,该步骤和实验操作 (选填“降温结晶”或“蒸发结晶”)的原理相似。
(4)当地人利用工具将卤水在室外风吹日晒一段时间后,浓度可提高至约17%,该步骤称为“晒卤”,应位于步骤 (选填“Ⅱ”、“Ⅲ”或“Ⅳ”)之后,请比较卓筒井手工制盐中“晒卤”和“煎盐”,两者的原理有何相似之处和不同之处 。

(1)“Ⅱ汲卤”获得卤水为悬浊液,溶液部分中氯化钠的浓度为7%,下表是氯化钠在不同温度时的溶解度。
| 温度(℃) | 20 | 40 | 60 | 80 |
| 氯化钠的溶解度(g/100g水) | 36.0 | 36.6 | 37.3 | 38.4 |
根据表中数据可得出:20℃时,氯化钠溶解度为 ,该卤水的溶液部分是氯化钠的 (选填“饱和”或“不饱和”)溶液。
(2)“Ⅲ滤卤”与实验操作过滤的原理一样其目的是为了分离溶液和 。
(3)“Ⅳ煎盐”用井中产生的天然气作为燃料,加热卤水,除去其中的溶剂,CH4燃烧的化学方程式是 ,该步骤和实验操作 (选填“降温结晶”或“蒸发结晶”)的原理相似。
(4)当地人利用工具将卤水在室外风吹日晒一段时间后,浓度可提高至约17%,该步骤称为“晒卤”,应位于步骤 (选填“Ⅱ”、“Ⅲ”或“Ⅳ”)之后,请比较卓筒井手工制盐中“晒卤”和“煎盐”,两者的原理有何相似之处和不同之处 。
20.实验室利用6.4g铜网制氧化铜,探究一氧化碳的还原性。实验装置如图(装置气密性良好,夹持仪器省略)。
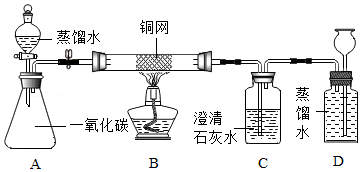
(1)关闭弹簧夹K,点燃酒精灯,铜网与装置内的氧气反应生成氧化铜,该反应的化学方程式是 。
(2)打开弹簧夹K,打开装置A中分液漏斗并控制蒸馏水流速平缓,目的是 ,一段时间后,B中铜网表面的现象是 ,说明一氧化碳具有还原性,此时C中的现象是 ,产生此现象的化学方程式是 。
(3)装置D的作用是 。
(4)为了能重复使用铜网,有人建议将铜网取出并称量,若质量 6.4g(选填“大于”“等于”或“小于”),说明铜网表面残留氧化铜,需完全除去后才能重复使用,你是否同意该方案,并阐述你的理由 。

(1)关闭弹簧夹K,点燃酒精灯,铜网与装置内的氧气反应生成氧化铜,该反应的化学方程式是 。
(2)打开弹簧夹K,打开装置A中分液漏斗并控制蒸馏水流速平缓,目的是 ,一段时间后,B中铜网表面的现象是 ,说明一氧化碳具有还原性,此时C中的现象是 ,产生此现象的化学方程式是 。
(3)装置D的作用是 。
(4)为了能重复使用铜网,有人建议将铜网取出并称量,若质量 6.4g(选填“大于”“等于”或“小于”),说明铜网表面残留氧化铜,需完全除去后才能重复使用,你是否同意该方案,并阐述你的理由 。
21.实验室常用3%的过氧化氢溶液制备氧气。
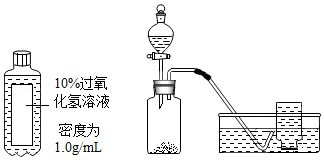
(1)欲配制100g 3%的过氧化氢溶液,需取用10%的过氧化氢溶液 mL。
(2)含0.04mol溶质的过氧化氢溶液完全反应,能产生多少克的氧气?(根据化学方程式列式计算)
(3)反应结束后,发生装置内剩余气体的主要成分为氧气,请设计实验方案,收集该剩余气体 。

(1)欲配制100g 3%的过氧化氢溶液,需取用10%的过氧化氢溶液 mL。
(2)含0.04mol溶质的过氧化氢溶液完全反应,能产生多少克的氧气?(根据化学方程式列式计算)
(3)反应结束后,发生装置内剩余气体的主要成分为氧气,请设计实验方案,收集该剩余气体 。
查看全部题目
相关试卷推荐
更多热门试卷
如何查看答案以及解析
扫描右侧二维码查看试卷答案解析以及视频讲解