下载高清试卷
2021-2022学年广东省茂名市电白区九年级(上)期末化学试卷
试卷格式:2021-2022学年广东省茂名市电白区九年级(上)期末化学试卷.PDF
试卷热词:最新试卷、2022年、广东试卷、茂名市试卷、化学试卷、九年级上学期试卷、期末试卷、初中试卷

扫码查看解析

扫码查看解析
扫码查看解析
扫码查看解析
扫码查看解析
扫码查看解析
扫码查看解析
扫码查看解析
试卷题目
1.劳动创造财富,劳动光荣。下列古诗中的劳动情景,涉及化学变化的是( )
- A. 锄禾日当午,汗滴禾下土
- B. 炉火照天地,红星乱紫烟
- C. 昼出耕田夜织麻,村庄儿女各当家
- D. 乡村四月闲人少,才了蚕桑又插秧
2.酒精运输车合适位置应张贴的标志是( )
- A.

- B.

- C.

- D.

3.2020年9月22日,我国对全球宣布:2030年前碳达峰,2060年前碳中和。实现这两个目标,碳循环必不可少,下列有关碳循环的说法错误的是( )
- A. 绿色植物光合作用吸收CO2释放O2
- B. 动、植物呼吸作用吸收O2释放CO2
- C. 用石灰水吸收空气中过量的CO2,以解决温室效应
- D. 提倡“低碳生活”,大力推广风能、太阳能等新能源
4.下列事实的结论或解释正确的是( )
- A. 水通电能产生氧气——说明水中含有氧分子
- B. 气体可压缩存储于钢瓶中——说明分子压缩后体积变小
- C. 金刚石和石墨物理性质差异很大——因为它们组成的元素不同
- D. 桂花开放时满园飘香——说明分子在不断运动
5.下列化学用语表示正确的是( )
- A. 2个钙离子:2Ca+2
- B. 1个水分子:H2O2
- C. 硫酸铁:FeSO4
- D. 五氧化二磷中磷元素化合价:2O5
+5 P
6.如图操作正确的是( )
- A.
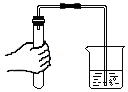 检查装置的气密性
检查装置的气密性 - B.
 闻气味
闻气味 - C.
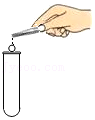 加入固体
加入固体 - D.
 过滤
过滤
7.分类法是化学研究的重要方法,以下分类错误的是( )
- A. 氧化物:水、二氧化锰、干冰
- B. 混合物:合金、冰水、液氧
- C. 金属:铁、铜、汞
- D. 清洁能源:太阳能、氢能、风能
8.下列关于碳及其化合物的说法,正确的是( )
- A. 二氧化碳能使用石蕊溶液染成紫色的干燥的纸花变红
- B. 与金刚石、石墨一样,活性炭是碳的另一种单质,物理和化学性质都相似
- C. 碳和一氧化碳的还原性,可用于冶金工业
- D. 二氧化碳和一氧化碳都可以使动物死亡,所以都有毒性
9.中学生应有一定的安全常识。下列做法不合理的是( )
- A. 高层楼房着火时,不乘坐电梯逃离
- B. 家用电器着火时,立即用水扑灭
- C. 室内起火时,不要急于打开所有门窗
- D. 实验时万一碰倒酒精灯引起燃烧,应立即用湿抹布盖灭
10.“生命至上、安全第一“,为及时发现天然气泄漏,某燃气公司常在天然气中加入少量具有特殊气味的乙硫酵(C2H5SH)。乙硫醇在空气中也能燃烧,乙硫醇燃烧的化学方程式为:2C2H5SH+9O2
4CO2+6H2O+2X.物质X的化学式为( )
| 点燃 |
- A. H2S
- B. SO2
- C. S2O4
- D. SO3
11.过氧乙酸(化学式为CH3COOOH)是一种杀菌能力较强的消毒剂,为预防新冠病毒,需在生活场所喷洒适量的过氧乙酸。下列关于过氧乙酸的说法正确的是( )
- A. 它是由碳、氢、氧三种元素组成的
- B. 过氧乙酸分子中含有氧气分子
- C. 它的相对分子质量为60
- D. 碳、氢、氧三种元素的质量比为2:4:3
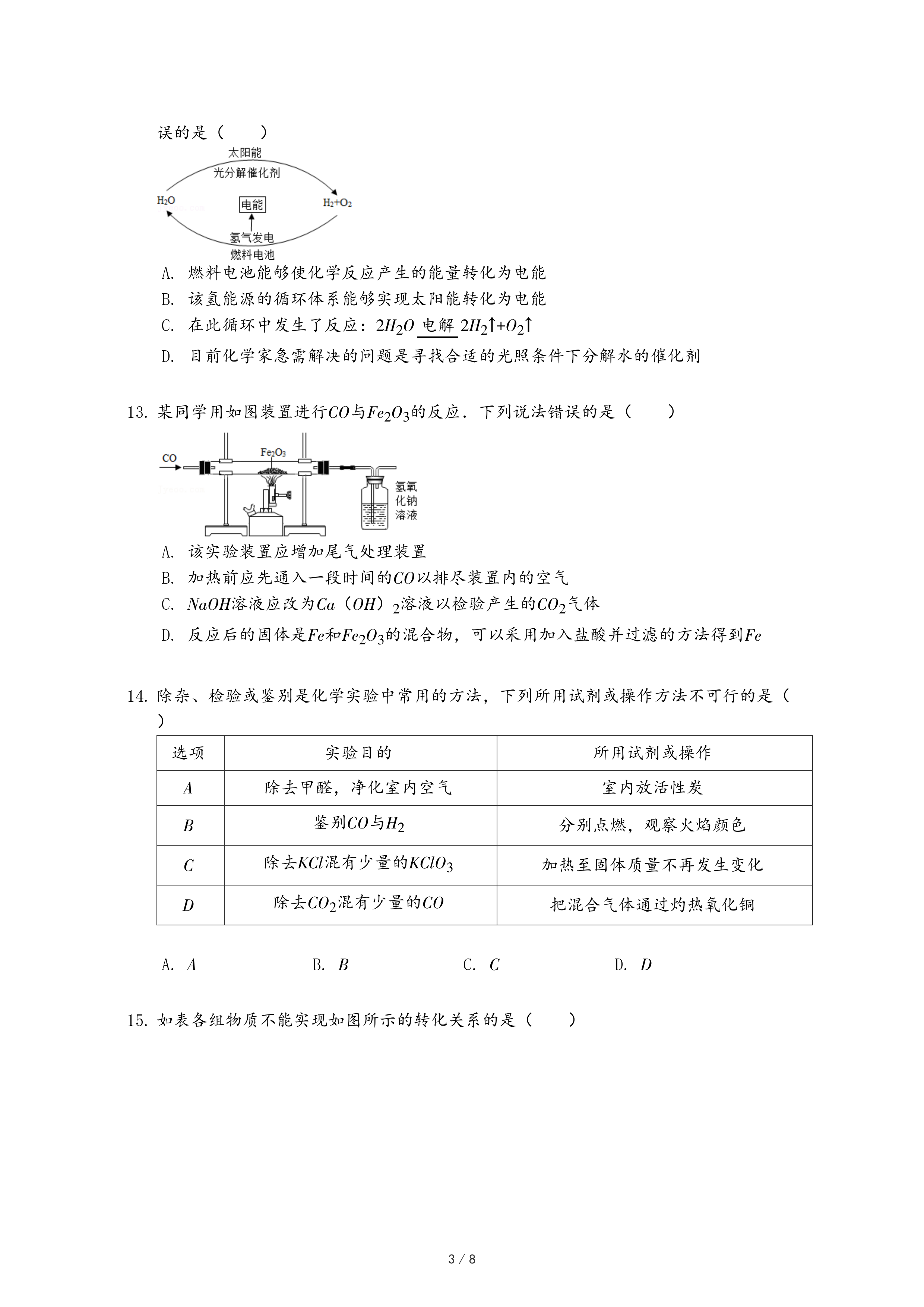
12.目前,科学家提出了一种最经济最理想的获得氢能源的循环体系(如图)。下列说法错误的是( )


- A. 燃料电池能够使化学反应产生的能量转化为电能
- B. 该氢能源的循环体系能够实现太阳能转化为电能
- C. 在此循环中发生了反应:2H2O2H2↑+O2↑
电解 - D. 目前化学家急需解决的问题是寻找合适的光照条件下分解水的催化剂
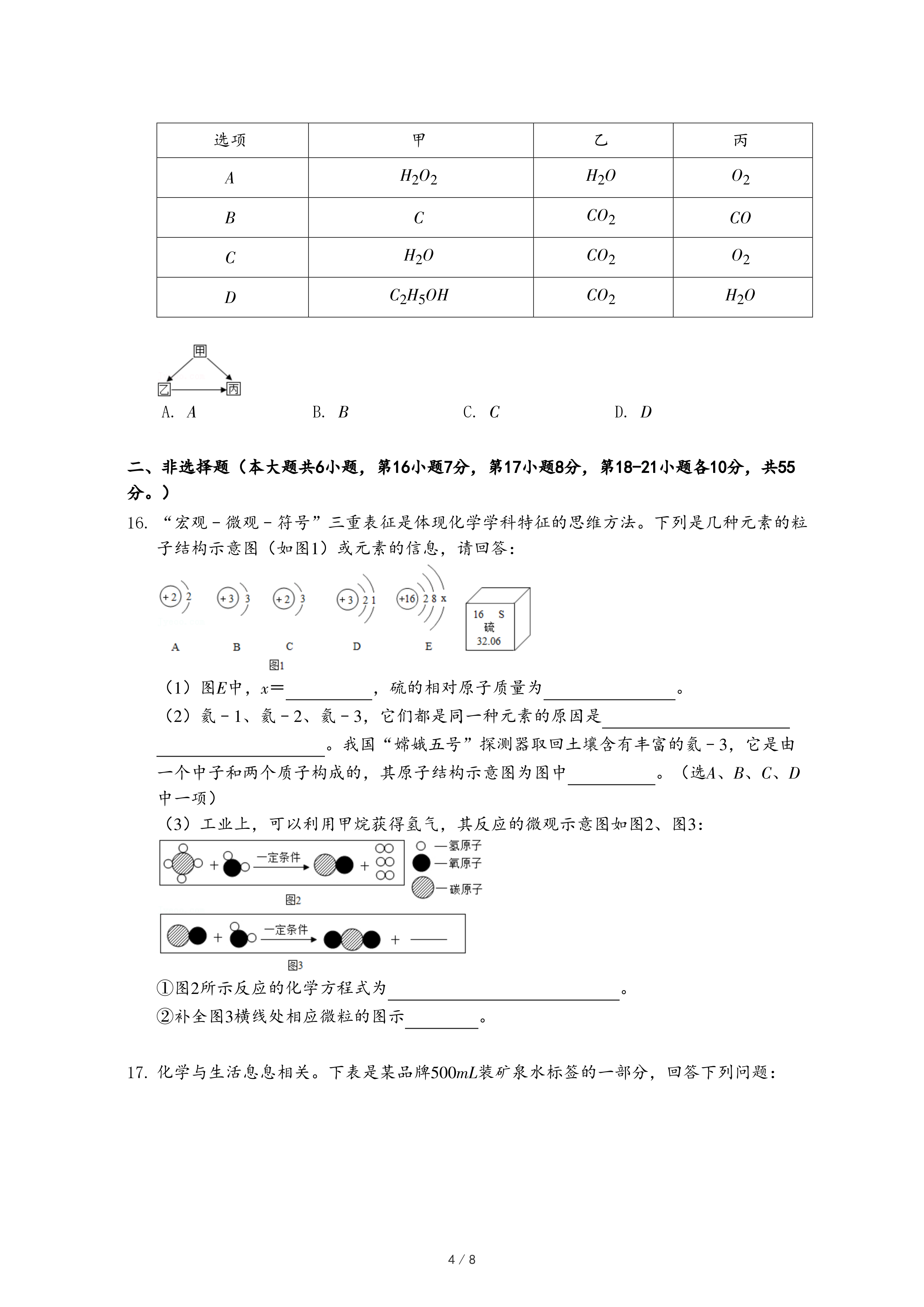
13.某同学用如图装置进行CO与Fe2O3的反应.下列说法错误的是( )
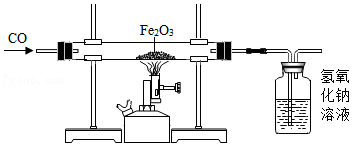

- A. 该实验装置应增加尾气处理装置
- B. 加热前应先通入一段时间的CO以排尽装置内的空气
- C. NaOH溶液应改为Ca(OH)2溶液以检验产生的CO2气体
- D. 反应后的固体是Fe和Fe2O3的混合物,可以采用加入盐酸并过滤的方法得到Fe
14.除杂、检验或鉴别是化学实验中常用的方法,下列所用试剂或操作方法不可行的是( )
| 选项 | 实验目的 | 所用试剂或操作 |
| A | 除去甲醛,净化室内空气 | 室内放活性炭 |
| B | 鉴别CO与H2 | 分别点燃,观察火焰颜色 |
| C | 除去KCl混有少量的KClO3 | 加热至固体质量不再发生变化 |
| D | 除去CO2混有少量的CO | 把混合气体通过灼热氧化铜 |
- A. A
- B. B
- C. C
- D. D
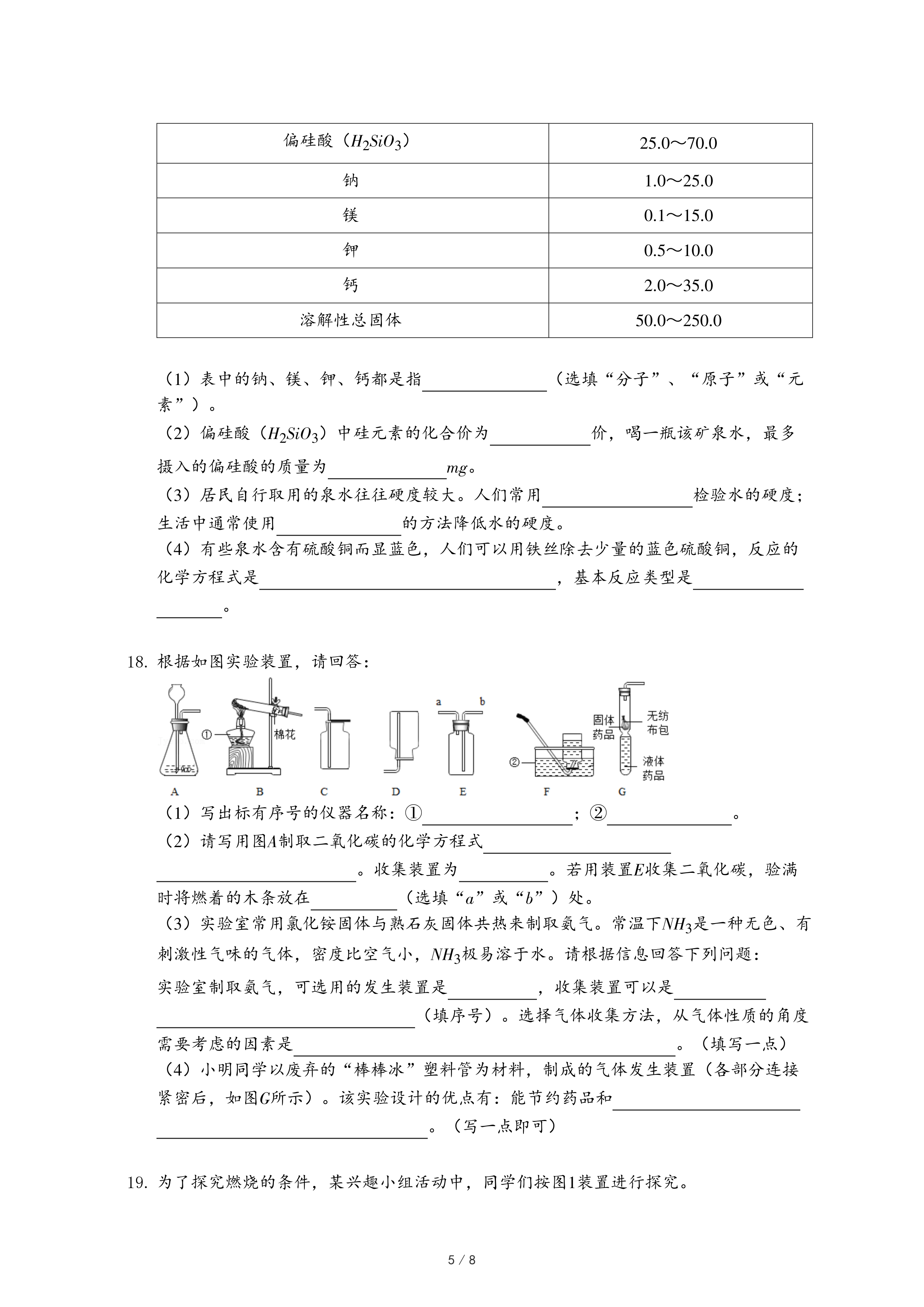
15.如表各组物质不能实现如图所示的转化关系的是( )
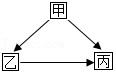
| 选项 | 甲 | 乙 | 丙 |
| A | H2O2 | H2O | O2 |
| B | C | CO2 | CO |
| C | H2O | CO2 | O2 |
| D | C2H5OH | CO2 | H2O |

- A. A
- B. B
- C. C
- D. D
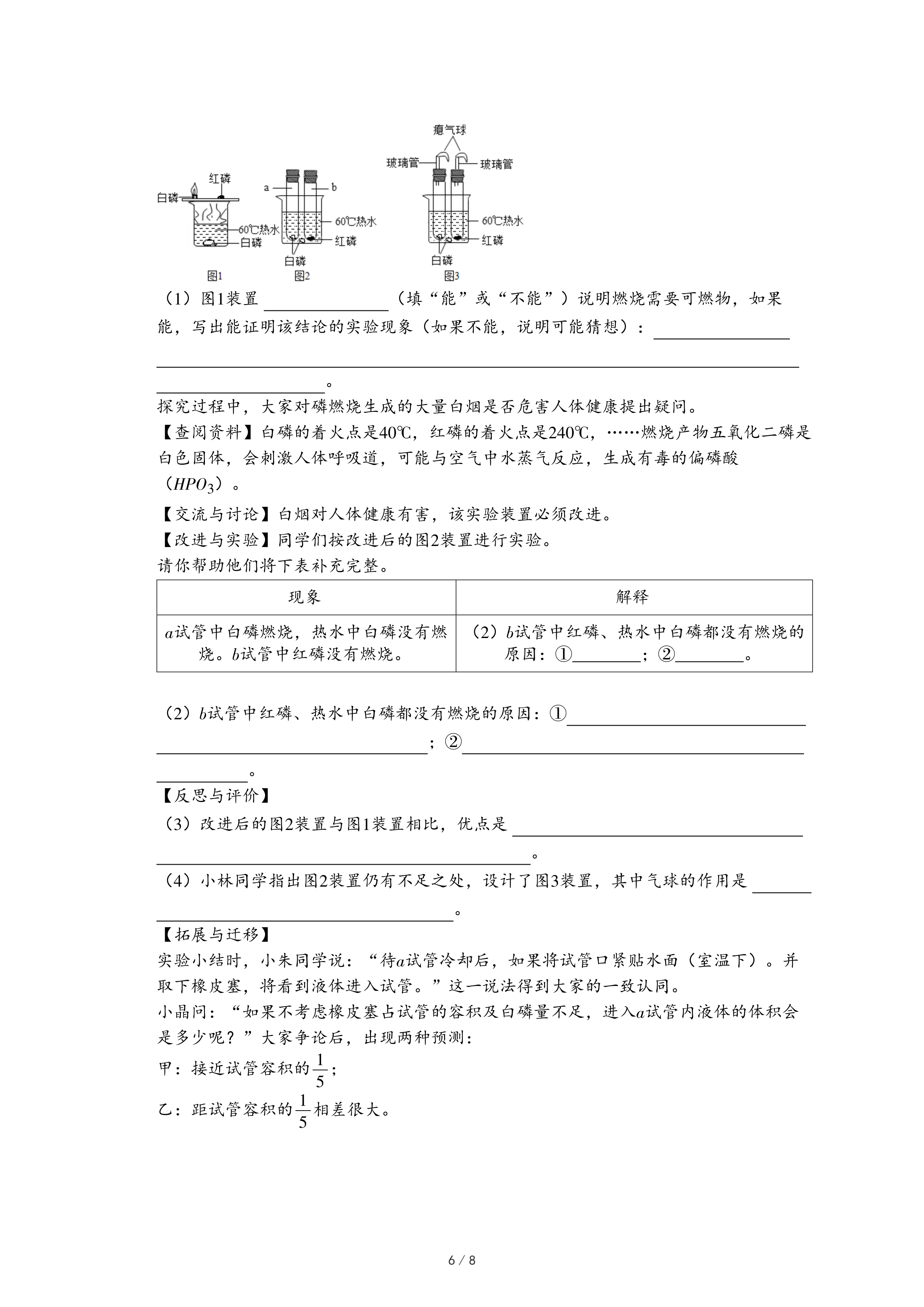
16.“宏观﹣微观﹣符号”三重表征是体现化学学科特征的思维方法。下列是几种元素的粒子结构示意图(如图1)或元素的信息,请回答:
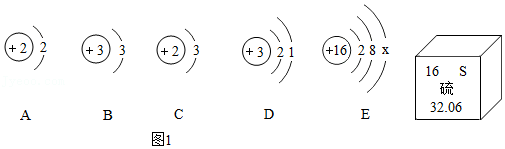
(1)图E中,x= ,硫的相对原子质量为 。
(2)氦﹣1、氦﹣2、氦﹣3,它们都是同一种元素的原因是 。我国“嫦娥五号”探测器取回土壤含有丰富的氦﹣3,它是由一个中子和两个质子构成的,其原子结构示意图为图中 。(选A、B、C、D中一项)
(3)工业上,可以利用甲烷获得氢气,其反应的微观示意图如图2、图3:
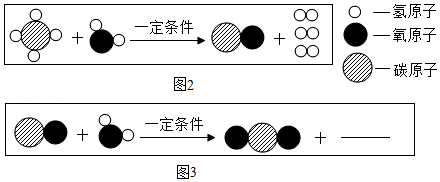
①图2所示反应的化学方程式为 。
②补全图3横线处相应微粒的图示 。

(1)图E中,x= ,硫的相对原子质量为 。
(2)氦﹣1、氦﹣2、氦﹣3,它们都是同一种元素的原因是 。我国“嫦娥五号”探测器取回土壤含有丰富的氦﹣3,它是由一个中子和两个质子构成的,其原子结构示意图为图中 。(选A、B、C、D中一项)
(3)工业上,可以利用甲烷获得氢气,其反应的微观示意图如图2、图3:

①图2所示反应的化学方程式为 。
②补全图3横线处相应微粒的图示 。
17.化学与生活息息相关。下表是某品牌500mL装矿泉水标签的一部分,回答下列问题:
(1)表中的钠、镁、钾、钙都是指 (选填“分子”、“原子”或“元素”)。
(2)偏硅酸(H2SiO3)中硅元素的化合价为 价,喝一瓶该矿泉水,最多摄入的偏硅酸的质量为 mg。
(3)居民自行取用的泉水往往硬度较大。人们常用 检验水的硬度;生活中通常使用 的方法降低水的硬度。
(4)有些泉水含有硫酸铜而显蓝色,人们可以用铁丝除去少量的蓝色硫酸铜,反应的化学方程式是 ,基本反应类型是 。
| 偏硅酸(H2SiO3) | 25.0~70.0 |
| 钠 | 1.0~25.0 |
| 镁 | 0.1~15.0 |
| 钾 | 0.5~10.0 |
| 钙 | 2.0~35.0 |
| 溶解性总固体 | 50.0~250.0 |
(1)表中的钠、镁、钾、钙都是指 (选填“分子”、“原子”或“元素”)。
(2)偏硅酸(H2SiO3)中硅元素的化合价为 价,喝一瓶该矿泉水,最多摄入的偏硅酸的质量为 mg。
(3)居民自行取用的泉水往往硬度较大。人们常用 检验水的硬度;生活中通常使用 的方法降低水的硬度。
(4)有些泉水含有硫酸铜而显蓝色,人们可以用铁丝除去少量的蓝色硫酸铜,反应的化学方程式是 ,基本反应类型是 。
18.根据如图实验装置,请回答:
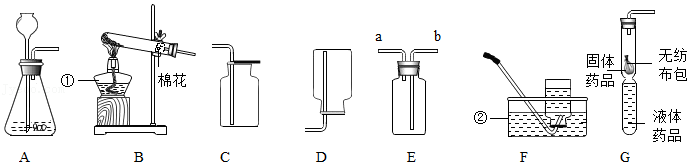
(1)写出标有序号的仪器名称:① ;② 。
(2)请写用图A制取二氧化碳的化学方程式 。收集装置为 。若用装置E收集二氧化碳,验满时将燃着的木条放在 (选填“a”或“b”)处。
(3)实验室常用氯化铵固体与熟石灰固体共热来制取氨气。常温下NH3是一种无色、有刺激性气味的气体,密度比空气小,NH3极易溶于水。请根据信息回答下列问题:
实验室制取氨气,可选用的发生装置是 ,收集装置可以是 (填序号)。选择气体收集方法,从气体性质的角度需要考虑的因素是 。(填写一点)
(4)小明同学以废弃的“棒棒冰”塑料管为材料,制成的气体发生装置(各部分连接紧密后,如图G所示)。该实验设计的优点有:能节约药品和 。(写一点即可)

(1)写出标有序号的仪器名称:① ;② 。
(2)请写用图A制取二氧化碳的化学方程式 。收集装置为 。若用装置E收集二氧化碳,验满时将燃着的木条放在 (选填“a”或“b”)处。
(3)实验室常用氯化铵固体与熟石灰固体共热来制取氨气。常温下NH3是一种无色、有刺激性气味的气体,密度比空气小,NH3极易溶于水。请根据信息回答下列问题:
实验室制取氨气,可选用的发生装置是 ,收集装置可以是 (填序号)。选择气体收集方法,从气体性质的角度需要考虑的因素是 。(填写一点)
(4)小明同学以废弃的“棒棒冰”塑料管为材料,制成的气体发生装置(各部分连接紧密后,如图G所示)。该实验设计的优点有:能节约药品和 。(写一点即可)
19.为了探究燃烧的条件,某兴趣小组活动中,同学们按图1装置进行探究。
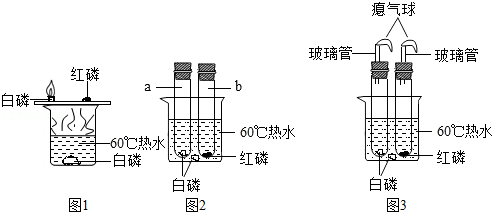
(1)图1装置 (填“能”或“不能”)说明燃烧需要可燃物,如果能,写出能证明该结论的实验现象(如果不能,说明可能猜想): 。
探究过程中,大家对磷燃烧生成的大量白烟是否危害人体健康提出疑问。
【查阅资料】白磷的着火点是40℃,红磷的着火点是240℃,……燃烧产物五氧化二磷是白色固体,会刺激人体呼吸道,可能与空气中水蒸气反应,生成有毒的偏磷酸(HPO3)。
【交流与讨论】白烟对人体健康有害,该实验装置必须改进。
【改进与实验】同学们按改进后的图2装置进行实验。
请你帮助他们将下表补充完整。
(2)b试管中红磷、热水中白磷都没有燃烧的原因:① ;② 。
【反思与评价】
(3)改进后的图2装置与图1装置相比,优点是 。
(4)小林同学指出图2装置仍有不足之处,设计了图3装置,其中气球的作用是 。
【拓展与迁移】
实验小结时,小朱同学说:“待a试管冷却后,如果将试管口紧贴水面(室温下)。并取下橡皮塞,将看到液体进入试管。”这一说法得到大家的一致认同。
小晶问:“如果不考虑橡皮塞占试管的容积及白磷量不足,进入a试管内液体的体积会是多少呢?”大家争论后,出现两种预测:
甲:接近试管容积的
;
乙:距试管容积的
相差很大。
(5)你赞同的预测是 (填“甲”或“乙”),理由是 。

(1)图1装置 (填“能”或“不能”)说明燃烧需要可燃物,如果能,写出能证明该结论的实验现象(如果不能,说明可能猜想): 。
探究过程中,大家对磷燃烧生成的大量白烟是否危害人体健康提出疑问。
【查阅资料】白磷的着火点是40℃,红磷的着火点是240℃,……燃烧产物五氧化二磷是白色固体,会刺激人体呼吸道,可能与空气中水蒸气反应,生成有毒的偏磷酸(HPO3)。
【交流与讨论】白烟对人体健康有害,该实验装置必须改进。
【改进与实验】同学们按改进后的图2装置进行实验。
请你帮助他们将下表补充完整。
| 现象 | 解释 |
| a试管中白磷燃烧,热水中白磷没有燃烧。b试管中红磷没有燃烧。 | (2)b试管中红磷、热水中白磷都没有燃烧的原因:①________;②________。 |
(2)b试管中红磷、热水中白磷都没有燃烧的原因:① ;② 。
【反思与评价】
(3)改进后的图2装置与图1装置相比,优点是 。
(4)小林同学指出图2装置仍有不足之处,设计了图3装置,其中气球的作用是 。
【拓展与迁移】
实验小结时,小朱同学说:“待a试管冷却后,如果将试管口紧贴水面(室温下)。并取下橡皮塞,将看到液体进入试管。”这一说法得到大家的一致认同。
小晶问:“如果不考虑橡皮塞占试管的容积及白磷量不足,进入a试管内液体的体积会是多少呢?”大家争论后,出现两种预测:
甲:接近试管容积的
| 1 |
| 5 |
乙:距试管容积的
| 1 |
| 5 |
(5)你赞同的预测是 (填“甲”或“乙”),理由是 。
20.电器的废旧电路板中往往含有Fe、Cu、Ag、Ni(镍,银白色金属,镍在盐溶液中一般显+2价),如图是某车间回收部分金属的工艺流程,已知:2Cu+O2+2H2SO4
2CuSO4+2H2O。

回答下列问题。
(1)操作①或②的名称为 。
(2)往滤液①中加入过量铁粉发生反应的化学方程式为 ,滤液②中的金属离子为 。
(3)滤渣③中含有的金属是 。
(4)根据以上工艺流程图,可以得出Ni、Fe的金属活动性强弱顺序是Ni Fe(填“>”或“<”)。
(5)滤液③中加入足量铁粉的主要目的是 。固体A除主要含有铜外,还含有一定量的铁,为了进一步提纯铜,可以向固体A中加入适量的稀硫酸,发生反应的化学方程式为 。
(6)相比于直接焚烧废旧电路板回收金属,该工艺流程的主要优点 。
| △ |

回答下列问题。
(1)操作①或②的名称为 。
(2)往滤液①中加入过量铁粉发生反应的化学方程式为 ,滤液②中的金属离子为 。
(3)滤渣③中含有的金属是 。
(4)根据以上工艺流程图,可以得出Ni、Fe的金属活动性强弱顺序是Ni Fe(填“>”或“<”)。
(5)滤液③中加入足量铁粉的主要目的是 。固体A除主要含有铜外,还含有一定量的铁,为了进一步提纯铜,可以向固体A中加入适量的稀硫酸,发生反应的化学方程式为 。
(6)相比于直接焚烧废旧电路板回收金属,该工艺流程的主要优点 。
21.胆矾(CuSO4•5H2O,相对分子质量为250)广泛应用于生产生活中。
(1)农药波尔多液由胆矾和石灰乳等配制而成。不能用铁桶来配制波尔多液,因为铁的金属活动性比铜的 (填“强”或“弱”)。
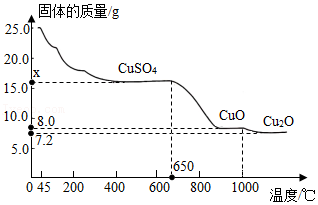
将25.0g胆矾放在坩埚内加热,固体质量与成分随温度变化的曲线如图。
(2)加热至 ℃时,CuSO4开始分解。
(3)加热至1000℃时,CuO开始分解,生成Cu2O与一种能使带火星的木条复燃的气体,该气体为 。CuO完全分解时产生该气体的质量为 g。
(4)根据胆矾分解的化学方程式CuSO4•5H2O
CuSO4+5H2O,计算图中x的值(写出计算过程)。
(5)下列物质均可作为炼铜的原料。理论上,冶炼等质量的下列物质得到铜最多的是 (填字母序号)。
a.CuSO4•5H2O
b.CuSO4
c.CuO
d.Cu2O
(1)农药波尔多液由胆矾和石灰乳等配制而成。不能用铁桶来配制波尔多液,因为铁的金属活动性比铜的 (填“强”或“弱”)。
将25.0g胆矾放在坩埚内加热,固体质量与成分随温度变化的曲线如图。
(2)加热至 ℃时,CuSO4开始分解。
(3)加热至1000℃时,CuO开始分解,生成Cu2O与一种能使带火星的木条复燃的气体,该气体为 。CuO完全分解时产生该气体的质量为 g。
(4)根据胆矾分解的化学方程式CuSO4•5H2O
| △ |
(5)下列物质均可作为炼铜的原料。理论上,冶炼等质量的下列物质得到铜最多的是 (填字母序号)。
a.CuSO4•5H2O
b.CuSO4
c.CuO
d.Cu2O

查看全部题目
相关试卷推荐
更多热门试卷
如何查看答案以及解析
扫描右侧二维码查看试卷答案解析以及视频讲解