下载高清试卷
【2020-2021学年北京市朝阳区九年级(上)期末化学试卷】-第1页
试卷格式:2020-2021学年北京市朝阳区九年级(上)期末化学试卷.PDF
试卷热词:最新试卷、2021年、北京试卷、朝阳区试卷、化学试卷、九年级上学期试卷、期末试卷、初中试卷
扫码查看解析
试卷题目
1.下列变化中,属于物理变化的是( )
- A. 粮食酿酒
- B. 瓷碗破碎
- C. 食物腐败
- D. 火药爆炸
2.下列食物富含蛋白质的是( )
- A. 鸡蛋
- B. 米饭
- C. 白菜
- D. 西瓜
3.下列元素中,因摄入量不足可能导致骨质疏松的是( )
- A. 铁
- B. 钠
- C. 钙
- D. 锌
4.空气成分中,体积分数最大的气体是( )
- A. 氮气
- B. 氧气
- C. 稀有气体
- D. 二氧化碳
5.下列物质在氧气中完全燃烧,生成黑色固体的是( )
- A. 木炭
- B. 铁丝
- C. 红磷
- D. 硫粉
6.下列属于有机合成材料的是( )
- A. 陶瓷
- B. 塑料保鲜膜
- C. 不锈钢
- D. 羊绒衫
7.下列实验操作正确的是( )
- A.
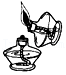 点燃酒精灯
点燃酒精灯 - B.
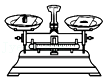 称量固体
称量固体 - C.
 滴加液体
滴加液体 - D.
 取用液体
取用液体
8.下列物质中,属于氧化物的是( )
- A. KCl
- B. NaOH
- C. SO2
- D. H2SO4
9.“含氟牙膏”中的“氟”指的是( )
- A. 元素
- B. 原子
- C. 分子
- D. 单质
10.下列净水方法中,净化程度最高的是( )
- A. 蒸馏
- B. 消毒
- C. 吸附
- D. 沉淀
11.食品包装中经常用到铝箔,铝能制成铝箔是因为铝具有( )
- A. 金属光泽
- B. 抗腐蚀性
- C. 导热性
- D. 延展性
12.明代宋应星所著的《天工开物》中记载的炼锡方法,用化学方程式表示为:SnO2+2C
Sn+2CO↑,该反应属于( )
| 高温 |
- A. 置换反应
- B. 分解反应
- C. 化合反应
- D. 复分解反应
13.用水壶烧开水,水沸腾后壶盖被顶起,说明( )
- A. 分子是由原子构成的
- B. 分子的质量很小
- C. 分子的体积变大
- D. 分子间空隙增大
14.下列符号表示“两个氢分子”的是( )
- A. H2
- B. H2O
- C. 2H2
- D. 2H
15.钠元素和氯元素的本质区别在于( )
- A. 相对原子质量不同
- B. 质子数不同
- C. 最外层电子数不同
- D. 中子数不同
16.下列图标中,表示“禁止烟火”的是( )
- A.

- B.

- C.

- D.

17.下列化学式书写正确的是( )
- A. 氧化铝 AlO
- B. 硫酸锌 ZnSO4
- C. 氯化铁 FeCl2
- D. 硝酸铜 CuNO3
18.密闭居室内使用燃气热水器容易使人中毒,使人中毒的气体是( )
- A. CO2
- B. CO
- C. O2
- D. N2
19.下列做法安全可行的是( )
- A. 电器着火,用水浇灭
- B. 高楼发生火灾,乘电梯逃生
- C. 在加油站拨打或接听移动电话
- D. 档案资料着火,用液态二氧化碳扑灭
20.下列关于物质用途的描述不正确的是( )
- A. 氧气可用作燃料
- B. 氮气可用于食品防腐
- C. 干冰可用于人工降雨
- D. 二氧化碳可用作气体肥料
21.钼主要用于航天合金材料制作。如图是钼元素在元素周期表中的信息,下列说法不正确的是( )
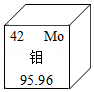

- A. 属于金属元素
- B. 相对原子质量为95.96g
- C. 原子核内质子数为42
- D. 原子核外电子数为42
22.绿茶中含有的单宁酸(C76H52O46)具有抑制血压上升、清热解毒等功效。下列有关单宁酸的说法正确的是( )
- A. 相对分子质量为174
- B. 由碳原子、氢分子和氧分子构成
- C. 氢元素的质量分数最小
- D. 碳、氧两种元素的质量比为76:46
23.下列实验得出的结论,正确的是( )
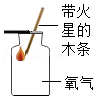 | 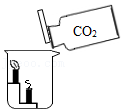 | 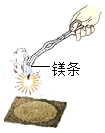 | 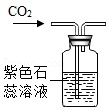 |
| A.氧气已收集满 | B.二氧化碳密度比空气大,不可燃也不助燃 | C.该实验可以验证质量守恒定律 | D.二氧化碳能与水反应 |
- A. A
- B. B
- C. C
- D. D
24.硼纤维具有较好的耐热性和弹性,不与氯气、水反应,可与某些金属制成新型材料。在1200℃~1300℃时,氯化硼(BCl3)蒸气与干燥、纯净的氢气反应可制得硼和氯化氢。下列说法不正确的是( )
- A. 含硼纤维的材料可能具有耐热性
- B. 氯化硼可能与水反应
- C. 该反应中只有两种物质为气态
- D. 该反应需要在隔绝空气的条件下进行
25.生产VR(虚拟现实)设备的材料之一是硅(Si),工业制取高纯硅的微观示意图如图。下列有关说法不正确的是( )
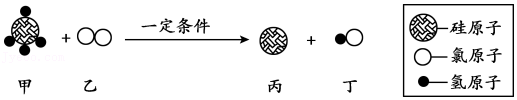

- A. 甲属于化合物
- B. 反应中乙和丁的分子个数比为1:2
- C. 反应前后氢、氯原子个数发生改变
- D. 参加反应的甲和乙的质量比为16:71
26.新能源汽车的发展对缓解能源危机和环境污染有重要作用。
(1)传统汽车采用化石燃料作为能源。化石燃料包括煤、 和天然气,天然气中甲烷燃烧的化学方程式为 。
(2)氢燃料电池车实现交通“零排放”的原因是 (用化学方程式解释)。
(1)传统汽车采用化石燃料作为能源。化石燃料包括煤、 和天然气,天然气中甲烷燃烧的化学方程式为 。
(2)氢燃料电池车实现交通“零排放”的原因是 (用化学方程式解释)。
27.金属与我们生活息息相关。
(1)泡沫铁粉可用于食品保鲜的原理:铁能吸收 ,从而使食品保持干燥并防止氧化变质。
(2)锈蚀钢铁回收重新冶炼是保护金属资源的一条有效途径。写出用CO还原锈蚀钢铁的化学方程式 。
(1)泡沫铁粉可用于食品保鲜的原理:铁能吸收 ,从而使食品保持干燥并防止氧化变质。
(2)锈蚀钢铁回收重新冶炼是保护金属资源的一条有效途径。写出用CO还原锈蚀钢铁的化学方程式 。
28.碳纤维是含碳量高于90%的新型材料,密度比铝小,强度比钢大。为了提高碳纤维的强度,必须选择适当的预氧化条件。将碳纤维进行预氧化处理,测得碳纤维强度与热处理温度的关系如图所示。
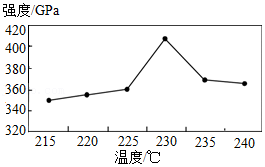
(1)碳纤维的物理性质有 。
(2)由图可知,碳纤维强度与热处理温度的关系是 。

(1)碳纤维的物理性质有 。
(2)由图可知,碳纤维强度与热处理温度的关系是 。
29.阅读下面科普短文。
“琉璃”与“玻璃”
“琉璃”与“玻璃”常被混为一谈。“琉璃”常指珍贵的饰品,“玻璃”制品在清中期以前常被误认为是“琉璃”制品。
琉璃与玻璃的成分、性能及用途
在古代,玻璃、有釉的陶器(如琉璃瓦)等都统称为“琉璃”。在明代景泰年间,工匠们把含有金属氧化物的二氧化硅碾成粉末,做成“涂料”,涂在铜胎上,高温炼制成琉璃艺术珍品﹣﹣景泰蓝。现今,“琉璃”则指用传统工艺制作的玻璃艺术品,多为手工制作。
玻璃是一种无规则结构的非晶态固体,没有固定的熔点。人们在普通玻璃中掺入某种金属氧化物,可以生产出有特定色彩的玻璃。例如,加入氧化钴使玻璃呈现蓝色,加入氧化亚铜使玻璃呈现红色,加入二氧化锰使玻璃呈现紫色等。将普通玻璃加热到700℃左右,再进行快速均匀的冷却就能得到钢化玻璃。钢化玻璃强度大、不容易破碎,即使破碎也会以无锐角的颗粒形式碎裂,对人体伤害大大降低。防盗玻璃为多层结构,每层中间嵌有极细的金属丝,当击碎玻璃时,与金属丝相连的电子警报系统立即发出报警信号。
总之,化学材料的研发将为人类社会的发展做出新的贡献。
依据文章内容回答下列问题:
(1)“琉璃”与“玻璃”均属于 (填“纯净物”或“混合物”)。
(2)“防盗玻璃”能报警,这是利用了金属的 。
(3)“琉璃”与“玻璃”的化学成分的主要区别是 (写出一条即可)。
(4)根据文中介绍的玻璃种类,私家车前挡风玻璃最好使用 。
(5)下列有关“琉璃”与“玻璃”的描述,正确的是 (填序号)。
A.“景泰蓝”是琉璃制品中的一种
B.玻璃属于非晶态固体,有固定的熔点
C.不同颜色的“玻璃”是因为其成分中含有不同的金属氧化物
D.化学仪器多为玻璃制作,是因为玻璃的透光度和折光率好
“琉璃”与“玻璃”
“琉璃”与“玻璃”常被混为一谈。“琉璃”常指珍贵的饰品,“玻璃”制品在清中期以前常被误认为是“琉璃”制品。
琉璃与玻璃的成分、性能及用途
| 名称 | 主要成分 | 其他成分 | 性能及用途 |
| 琉璃 | 二氧化硅最多达到90% | 金属氧化物(氧化铝、氧化钴、氧化铅)约8%~10% | 具有特殊的金属色泽,可用于制作流光溢彩的饰品、有釉的陶制建筑用品等 |
| 玻璃 | 二氧化硅92%~99% | 金属氧化物(氧化钙、氧化铅)只占1%左右 | 具有非常好的透光度和折光率,可生产试管、烧杯等化学仪器 |
在古代,玻璃、有釉的陶器(如琉璃瓦)等都统称为“琉璃”。在明代景泰年间,工匠们把含有金属氧化物的二氧化硅碾成粉末,做成“涂料”,涂在铜胎上,高温炼制成琉璃艺术珍品﹣﹣景泰蓝。现今,“琉璃”则指用传统工艺制作的玻璃艺术品,多为手工制作。
玻璃是一种无规则结构的非晶态固体,没有固定的熔点。人们在普通玻璃中掺入某种金属氧化物,可以生产出有特定色彩的玻璃。例如,加入氧化钴使玻璃呈现蓝色,加入氧化亚铜使玻璃呈现红色,加入二氧化锰使玻璃呈现紫色等。将普通玻璃加热到700℃左右,再进行快速均匀的冷却就能得到钢化玻璃。钢化玻璃强度大、不容易破碎,即使破碎也会以无锐角的颗粒形式碎裂,对人体伤害大大降低。防盗玻璃为多层结构,每层中间嵌有极细的金属丝,当击碎玻璃时,与金属丝相连的电子警报系统立即发出报警信号。
总之,化学材料的研发将为人类社会的发展做出新的贡献。
依据文章内容回答下列问题:
(1)“琉璃”与“玻璃”均属于 (填“纯净物”或“混合物”)。
(2)“防盗玻璃”能报警,这是利用了金属的 。
(3)“琉璃”与“玻璃”的化学成分的主要区别是 (写出一条即可)。
(4)根据文中介绍的玻璃种类,私家车前挡风玻璃最好使用 。
(5)下列有关“琉璃”与“玻璃”的描述,正确的是 (填序号)。
A.“景泰蓝”是琉璃制品中的一种
B.玻璃属于非晶态固体,有固定的熔点
C.不同颜色的“玻璃”是因为其成分中含有不同的金属氧化物
D.化学仪器多为玻璃制作,是因为玻璃的透光度和折光率好
30.金属钨(W)可做白炽灯泡的灯丝,用黑钨矿[主要含有钨酸亚铁(FeWO4)]制得金属钨的工艺流程如图所示。
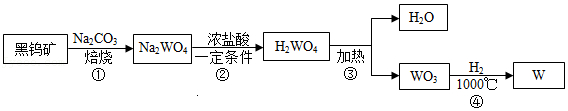
已知:WO3是难溶于水的固体
(1)FeWO4中钨元素的化合价为 。
(2)反应②的化学方程式为:Na2WO4+2HCl
H2WO4+2X,X的化学式为 。
(3)反应③的化学方程式为 。

已知:WO3是难溶于水的固体
(1)FeWO4中钨元素的化合价为 。
(2)反应②的化学方程式为:Na2WO4+2HCl
| 一定条件 |
(3)反应③的化学方程式为 。
31.工业上用石灰石为原料制备纳米CaCO3的一种流程如图所示。
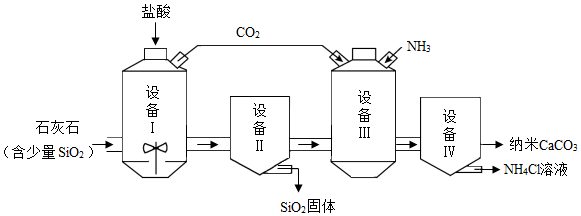
已知:SiO2不与盐酸反应
(1)设备Ⅰ中需不断搅拌,其目的是 。设备Ⅰ中发生反应的化学方程式为 。
(2)设备Ⅱ和设备Ⅳ均为分离设备,设备Ⅳ中的分离操作是 。
(3)设备Ⅲ中参加反应的物质除水外,还有 。

已知:SiO2不与盐酸反应
(1)设备Ⅰ中需不断搅拌,其目的是 。设备Ⅰ中发生反应的化学方程式为 。
(2)设备Ⅱ和设备Ⅳ均为分离设备,设备Ⅳ中的分离操作是 。
(3)设备Ⅲ中参加反应的物质除水外,还有 。
32.根据如图所示实验,回答问题。
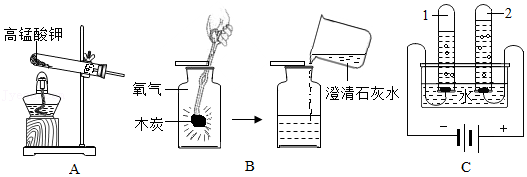
(1)实验A,发生反应的化学方程式为 ,能用排水法收集氧气的原因是 。
(2)实验B,能说明木炭燃烧的产物为二氧化碳的依据是 (用化学方程式表示)。
(3)实验C,试管2中产生的气体是 ,该实验证明水由 组成。

(1)实验A,发生反应的化学方程式为 ,能用排水法收集氧气的原因是 。
(2)实验B,能说明木炭燃烧的产物为二氧化碳的依据是 (用化学方程式表示)。
(3)实验C,试管2中产生的气体是 ,该实验证明水由 组成。
33.根据如图所示实验,回答问题。
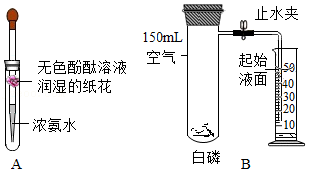
(1)实验A能说明氨分子不断运动的实验现象是 ,该实验说明浓氨水具有 性。
(2)实验B验证了空气中氧气的含量,白磷的作用是 ,白磷熄灭、试管冷却后再打开止水夹,水倒流入试管中,最终量筒中液面约降至 mL刻度线处,原因是 。

(1)实验A能说明氨分子不断运动的实验现象是 ,该实验说明浓氨水具有 性。
(2)实验B验证了空气中氧气的含量,白磷的作用是 ,白磷熄灭、试管冷却后再打开止水夹,水倒流入试管中,最终量筒中液面约降至 mL刻度线处,原因是 。
34.利用如图装置探究“温度达到着火点是可燃物燃烧的条件之一”。实验中观察到甲中白磷燃烧,乙中白磷不燃烧。
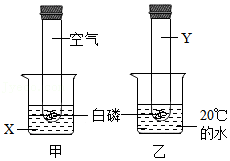
已知:白磷的着火点是40℃
(1)甲中白磷燃烧的化学方程式为 。
(2)甲中的X、乙中的Y分别为 。
(3)若验证可燃物燃烧的另一个条件,还需要补充的实验是 。

已知:白磷的着火点是40℃
(1)甲中白磷燃烧的化学方程式为 。
(2)甲中的X、乙中的Y分别为 。
(3)若验证可燃物燃烧的另一个条件,还需要补充的实验是 。
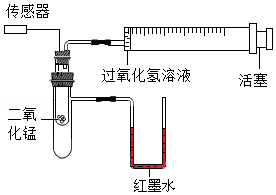
35.化学小组利用如图所示装置进行实验。
(1)小试管中发生反应的化学方程式为 。
(2)设计实验①和实验②的目的是 。
(3)实验过程中,还观察到U型管右侧液面均上升,依据此现象可推测该反应是 反应。
| 实验装置 | 实验药品 | 实验数据 | ||
 | 过氧化氢溶液 | 二氧化锰 | 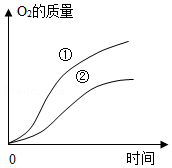 | |
| ① | 10mL 3.4% | 0.2g | ||
| ② | 10mL 2.4% | 0.2g | ||
(1)小试管中发生反应的化学方程式为 。
(2)设计实验①和实验②的目的是 。
(3)实验过程中,还观察到U型管右侧液面均上升,依据此现象可推测该反应是 反应。
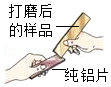
36.小组同学收集了某种铝制易拉罐,剪成条状并打磨后进行如图所示实验,发现纯铝片表面有划痕。
【发现问题】结合上述现象,可得出该易拉罐不是纯铝制作。那么易拉罐中除铝外,还含有什么金属呢?
【查阅资料】①铝制易拉罐中的主要成分是铝,可能还含有镁、铁。
②铝能与氢氧化钠溶液反应:2Al+2NaOH+2H2O═2NaAlO2+3H2↑;镁和铁不能与氢氧化钠溶液反应。
【猜想与假设】该易拉罐中除铝外,可能还含有镁、铁中的一种或两种。
【进行实验】小明取打磨后的铝制易拉罐样品按如下方案进行实验:
【解释与结论】
(1)纯铝片表面有划痕,说明合金的硬度比组成它的纯金属更 。
(2)实验1中,加入的溶液A是 溶液。
(3)实验2中,能证明样品中含有铁的实验现象是 。
【反思与评价】
(4)其他同学分析后认为小明的实验方案不严谨,理由是 。
(5)大家认为应该补充下列实验:取实验1中少量黑色固体于试管中,加入某种金属的化合物溶液,若无现象,则小明的结论正确。你认为加入的金属化合物溶液中的金属元素可能是 (填一种即可)。
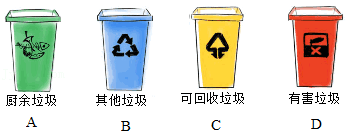
(6)废弃易拉罐应放入标有 (填序号)图标的垃圾桶内。
【发现问题】结合上述现象,可得出该易拉罐不是纯铝制作。那么易拉罐中除铝外,还含有什么金属呢?
【查阅资料】①铝制易拉罐中的主要成分是铝,可能还含有镁、铁。
②铝能与氢氧化钠溶液反应:2Al+2NaOH+2H2O═2NaAlO2+3H2↑;镁和铁不能与氢氧化钠溶液反应。
【猜想与假设】该易拉罐中除铝外,可能还含有镁、铁中的一种或两种。
【进行实验】小明取打磨后的铝制易拉罐样品按如下方案进行实验:
| 实验步骤 | 实验现象 | 实验结论 | |
| 实验1 | 取一定量的样品于烧杯中,加入足量的溶液A,充分反应 | 产生大量气泡,烧杯底部有黑色固体剩余 | 样品中含铝 |
| 实验2 | 取实验1中少量黑色固体于试管中,加入足量的稀盐酸 | 固体消失,产生气泡,溶液变为浅绿色 | 样品中含铁 |
【解释与结论】
(1)纯铝片表面有划痕,说明合金的硬度比组成它的纯金属更 。
(2)实验1中,加入的溶液A是 溶液。
(3)实验2中,能证明样品中含有铁的实验现象是 。
【反思与评价】
(4)其他同学分析后认为小明的实验方案不严谨,理由是 。
(5)大家认为应该补充下列实验:取实验1中少量黑色固体于试管中,加入某种金属的化合物溶液,若无现象,则小明的结论正确。你认为加入的金属化合物溶液中的金属元素可能是 (填一种即可)。
(6)废弃易拉罐应放入标有 (填序号)图标的垃圾桶内。


37.《梦溪笔谈》中记录了在用铁釜盛装硫酸铜溶液熬制硫酸铜晶体时,铁釜用久了会化作铜。
(1)由上述材料可知,铁比铜的金属活动性 。
(2)向足量的硫酸铜溶液中加入11.2g铁粉,充分反应后,理论上可以得到铜的质量是多少?
(1)由上述材料可知,铁比铜的金属活动性 。
(2)向足量的硫酸铜溶液中加入11.2g铁粉,充分反应后,理论上可以得到铜的质量是多少?
查看全部题目
相关试卷推荐
更多热门试卷
如何查看答案以及解析
扫描右侧二维码查看试卷答案解析以及视频讲解